题目内容
取五等份NO2 ,分别加入温度不同、容积相同的恒容密闭容器中,发生反应:
2NO2(g)  N2O4(g) ΔH<0 反应相同时间后,分别测定体系中NO2的百分含量(NO2%),并作出其随反应温度(T)变化的关系图。下列示意图中,可能与实验结果相符的是
N2O4(g) ΔH<0 反应相同时间后,分别测定体系中NO2的百分含量(NO2%),并作出其随反应温度(T)变化的关系图。下列示意图中,可能与实验结果相符的是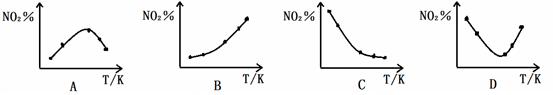
BD
解析试题分析:A.该反应是放热反应,温度越高,平衡向逆反应方向移动,NO2的百分含量随温度升高而升高,A错误;B.该反应是放热反应,温度越高,平衡向逆反应方向移动,NO2的百分含量随温度升高而升高,B正确;C.若5个容器中有未达到平衡状态的,那么温度越高,反应速率越大,会出现温度高的NO2转化得快,导致NO2的百分含量少的情况,不可能出现NO2的百分含量的情况,C错误;D.在D图中转折点为平衡状态,转折点左则为未平衡状态,右则为平衡状态,反应是放热反应,温度升高,平衡向逆反应方向移动,故D正确
考点:体积百分含量随温度、压强变化曲线

练习册系列答案
相关题目
判断一个化学反应的自发性常用焓判据和熵判据,则在下列情况下,可以判定反应一定自发进行的是( )
| A.ΔH>0,ΔS>0 | B.ΔH<0,ΔS<0 |
| C.ΔH>0,ΔS<0 | D.ΔH<0,ΔS>0 |
某温度下,X(g)+Y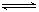 2Z反应达到平衡,在升高温度或减小压强的情况下,平衡均向右移动,则下列有关反应的各种叙述中正确的是
2Z反应达到平衡,在升高温度或减小压强的情况下,平衡均向右移动,则下列有关反应的各种叙述中正确的是
| A.正反应是吸热反应,Z是固体 |
| B.逆反应是放热反应,Y是固体,Z为气体 |
| C.正反应是吸热反应,只有Z不是气体 |
| D.正反应是放热反应,Y和Z均为气体 |
在一密闭容器中充入一定量的N2和H2,经测定反应开始后的2s内氢气的平均速率:ν(H2)=0.45mol/(L·s),则2s末NH3,的浓度为
| A.0.50mol/L | B.0.60mol/L | C.0.45mol/L | D.0.55mol/L |
设C+CO2  2CO(正反应为吸热反应),反应速率为υ1;N2+3H2
2CO(正反应为吸热反应),反应速率为υ1;N2+3H2 2NH3(正反应为放热反应),反应速率为υ2,对于上述反应,当温度升高时,υ1和υ2的变化情况为
2NH3(正反应为放热反应),反应速率为υ2,对于上述反应,当温度升高时,υ1和υ2的变化情况为
| A.同时增大 | B.同时减小 | C.υ1增大,υ2减小 | D.υ1减小,υ2增大 |
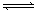 2AB3(g) △H<0(正反应放热),下列图像(其中W为质量分数)不正确的是 ( )
2AB3(g) △H<0(正反应放热),下列图像(其中W为质量分数)不正确的是 ( )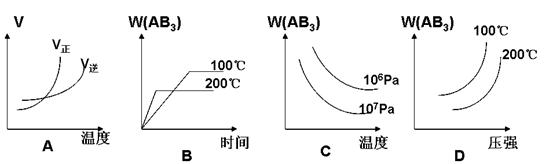
 B(g)(正反应为吸热反应)在密闭容器中达到平衡,平衡后c(A)/c(B)=a,若改变某一条件,足够时间后反应再次达到平衡状态,此时c(A)/c(B)=b,下列叙述正确的是 ( )
B(g)(正反应为吸热反应)在密闭容器中达到平衡,平衡后c(A)/c(B)=a,若改变某一条件,足够时间后反应再次达到平衡状态,此时c(A)/c(B)=b,下列叙述正确的是 ( ) 2CO; △H1>0,反应速率ν1 N2+3H2
2CO; △H1>0,反应速率ν1 N2+3H2 和
和 的变化是
的变化是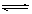 2CO; △H1>0,反应速率ν1 N2+3H2
2CO; △H1>0,反应速率ν1 N2+3H2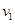 和
和 的变化是
的变化是