题目内容
【题目】“8.12”天津港爆炸中有一定量的氰化物泄露.氰化物多数易溶于水,有剧毒,易造成水污染.为了增加对氰化物的了解,同学们查找资料进行学习和探究。
探究氰化物的性质:已知部分弱酸的电离平衡常数如下表:
弱酸 | HCOOH | HCN | H2CO3 |
25℃电离平衡常数 | Ki=1.77×10﹣4 | Ki=5.0×10﹣10 | Ki1=4.3×10﹣7 Ki2=5.6×10﹣11 |
(1)NaCN溶液呈碱性的原因是________________________ (用离子方程式表示)
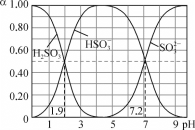
(2)如图表示常温下,稀释HCOOH、HCN两种酸的稀溶液时,溶液pH随加水量的变化.下列说法正确的是_________

A.相同浓度的HCOONa和NaCN的混合溶液中,各离子浓度的大小关系是:c(Na+)>c(CN﹣)>c(HCOO﹣)>c(OH﹣)>c(H+)
B.向NaCN溶液中通入少量二氧化碳的离子方程式为:CN﹣+CO2+H2O=HCN+CO32﹣
C.图像中a点酸的总浓度小于b点酸的总浓度
D.c点溶液的导电性比a点溶液的导电性弱
(3)H2O2有“绿色氧化剂”的美称;也可消除水中的氰化物(如KCN),经以下反应实现:KCN+H2O2+H2O═A+NH3↑,则生成物A的化学式为_____。
(4)下列四种离子结合H+能力由弱到强的是______________________________________。
A. HCOO- B. CN- C. CO32- D.HCO3-
【答案】CN﹣+H2OHCN+OH﹣ CD KHCO3 A<D<B<C
【解析】
(1)NaCN为强碱弱酸盐,CN-发生水解:CN-+H2O![]() HCN+OH-,c(OH-)>c(H+),使溶液显碱性;
HCN+OH-,c(OH-)>c(H+),使溶液显碱性;
(2)A、根据表中数据,酸性:HCOOH>HCN,即CN-水解程度大于HCOO-,离子浓度大小顺序是c(Na+)>c(HCOO-)>c(CN-)>c(OH-)>c(H+),故A错误;
B、电离出H+能力:H2CO3>HCN>HCO3-,通入少量CO2反应离子方程式为:CN-+CO2+H2O=HCN+HCO3-,故B错误;
C、根据表格数据,HCOOH的酸性强于HCN,相同pH时,稀释相同倍数,酸性强的pH变化大,即曲线I代表HCOOH,开始时pH相同,c(HCOOH)>c(HCN),故C正确;
D、电解质溶液导电能力与离子浓度、所带电荷数有关,c点离子浓度小于a点,即c点溶液的导电性比a点溶液的导电性弱,故D正确;
(3)利用原子守恒,推出A的化学式为KHCO3;
(4)根据表格中数据,电离出H+能力:HCOOH>H2CO3>HCN>HCO3-,利用越弱越水解,推出结合H+能力由弱到强的顺序是HCOO-<HCO3-<CN-<CO32-,即A<D<B<C。

 教材全解字词句篇系列答案
教材全解字词句篇系列答案【题目】25℃时,浓度均为0.1mol/L的溶液,其pH如下表所示。有关说法正确的是
序号 | ① | ② | ③ | ④ |
溶液 |
|
|
|
|
pH | 7.0 | 7.0 | 8.1 | 8.9 |
A. 酸性强弱: ![]()
B. 离子的总浓度:①>③
C. ②中: ![]()
D. ②和④中![]() 相等
相等