题目内容
3.下列事实中,不能用勒•沙特列原理解释的是( )| A. | 红棕色的NO2加压后颜色先变深后变浅(已知:2NO2 (g)?N2O4 (g)) | |
| B. | 实验室中常用排饱和食盐水的方法收集氯气 | |
| C. | 对H2(g)+I2(g)?2HI(g),平衡体系增大压强可使颜色变深 | |
| D. | 工业上生产硫酸的过程中使用过量的空气以提高二氧化硫的利用率 |
分析 勒夏特列原理为:如果改变影响平衡的条件之一,平衡将向着能够减弱这种改变的方向移动;
使用勒夏特列原理时,研究对象必须为可逆反应,否则勒夏特列原理不适用;
催化剂只能改变反应速率,不会影响化学平衡,所以不能用勒夏特列原理解释.
解答 解:A、可以可逆反应2NO2(g)?N2O4(g),正反应为体积缩小的反应,加压后二氧化氮的浓度增大,所以气体有色加深,由于增大了压强,平衡向生成四氧化二氮的方向移动,故加压后颜色先变深后变浅,可以平衡移动原理解释,故A错误;
B、实验室可用排饱和食盐水的方法收集氯气,氯气和水的反应是可逆反应,饱和氯化钠溶液中氯离子浓度大,化学平衡逆向进行,减小氯气溶解度,能用勒沙特列原理解释,故B错误;
C、气体两边的计量数相等,增加压强平衡不移动,不能利用勒夏特列原理解释,故C正确;
D、工业上生产硫酸存在平衡2SO2+O2?2SO3,使用过量的空气,增大氧气的浓度,平衡向正反应移动,可以提高二氧化硫的利用率,能用勒夏特列原理解释,故D错误,故选C.
点评 本题考查勒夏特列原理知识,题目难度不大,注意使用勒夏特列原理的前提必须是可逆反应,且是否发生平衡的移动.

练习册系列答案
相关题目
15.下列离子方程式中,正确的是( )
| A. | 稀硫酸滴在铜片上:Cu+2H+═Cu2++H2↑ | |
| B. | 铜片插入硝酸银溶液中:Cu+Ag+═Cu2++Ag | |
| C. | 稀盐酸与碳酸钠溶液反应:2H++CO32-═H2O+CO2↑ | |
| D. | 将铁粉加入稀硫酸中:2Fe+6 H+═2Fe3++3 H2↑ |
12.下列说法中正确的是( )
| A. | 向饱和Na2CO3溶液中通入过量的CO2,溶液中无明显现象 | |
| B. | 将8 g SO3 放入92 g水中,所得溶液溶质质量分数为8% | |
| C. | 已知H+(aq)+OH-(aq)═HO(l);△H=-57.3 kJ/mol.将4 g氢氧化钠固体放入100 mL 1 mol/L的稀盐酸中,放出了5.73 kJ的热量 | |
| D. | 向100 ml 1 mol/L的Ca(HCO3)2 溶液中加入等浓度等体积的NaOH溶液,溶液的碱性减弱 |
18.某无色透明酸性溶液中,能大量共存的离子组是( )
| A. | Na+、CO32-、Cu2+、SO42- | B. | K+、Fe3+、SO42-、OH- | ||
| C. | Ca2+、NO3-、Cl-、K+ | D. | Ba2+、K+、MnO4-、NO3- |
10.关于蛋白质的下列叙述正确的是( )
| A. | 加热会使蛋白质变性,因此生吃鸡蛋比熟吃好 | |
| B. | 蛋白质水解时直接变成氨基酸 | |
| C. | 一束光线照射蛋白质溶液,产生丁达尔效应 | |
| D. | 蛋白质仅含C、H、O、N四种元素 |
8.已知反应2X+Y═3Z+W在某段时间内以Y表示的化学反应速率为0.3mol/(L•min),此段时间内以Z的浓度变化表示的化学反应速率为( )
| A. | 0.3mol/(L•min) | B. | 0.6mol/(L•min) | C. | 0.9mol/(L•min) | D. | 1.2mol/(L•min) |
 A、B、C、D、E、F为前四周期的元素.其中,A元素和B元素的原子都有一个未成对电子,A3+比B-少一个电子层,B原子得一个电子后3p轨道全充满;C原子的p轨道中有3个未成对电子,其气态氢化物在水中的溶解性在同族元素所形成的氢化物中最大;D的最高化合价与最低化合价代数和为4,其最高价氧化物对应的水化物可以用于制取炸药和制作铅蓄电池;E元素的基态原子核外有六种运动状态的电子;F元素的单质为红色固体,可通过“湿法冶金”而得.请回答下列问题:
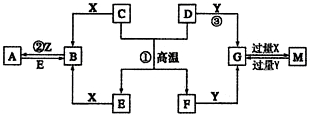
A、B、C、D、E、F为前四周期的元素.其中,A元素和B元素的原子都有一个未成对电子,A3+比B-少一个电子层,B原子得一个电子后3p轨道全充满;C原子的p轨道中有3个未成对电子,其气态氢化物在水中的溶解性在同族元素所形成的氢化物中最大;D的最高化合价与最低化合价代数和为4,其最高价氧化物对应的水化物可以用于制取炸药和制作铅蓄电池;E元素的基态原子核外有六种运动状态的电子;F元素的单质为红色固体,可通过“湿法冶金”而得.请回答下列问题: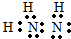 .
.
 .
.