题目内容
13.如图表示各物质之间的转化关系.已知D、E、Z是中学化学常见的单质,其他都是化合物.Z、Y是氯碱工业的产品.D元素的原子最外层电子数与电子层数相等,且D的硫酸盐可作净水剂.E为日常生活中应用最广泛的金属.除反应①外,其他反应均在水溶液中进行.请回答下列问题.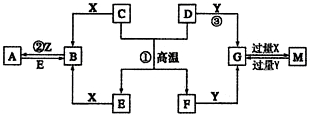
(1)写出X的电子式:
 .
.(2)常温时pH=12的G溶液中,溶质的阳离子与溶质的阴离子浓度之差为(10-2-10-12)mol/L(写出计算式).
(3)在电镀工业中,若将E作为待镀金属,铜为镀层金属,则铜是阳极,请写出在E电极上发生的电极反应式:Cu2++2e-=Cu.
(4)写出反应③的离子方程式:2Al+2OH-+2H2O=2AlO2-+3H2↑.
(5)现有无标签的Y和M的两种无色水溶液,不用其他任何试剂,请你设计一个简单的实验对这两种溶液加以鉴别Y中滴加M,先没有沉淀后生成沉淀,而M中滴加Y,先生成沉淀后沉淀消失,则Y为NaOH,M为AlCl3(回答实验操作、现象及结论).
(6)A溶液与NaOH溶液混合可形成沉淀,某温度下此沉淀的Ksp=2.097×l0-39.将0.01mol/L的A溶液与0.001mol•L-1的NaOH溶液等体积混合,你认为能否形成沉淀能(填“能”或“不能”),请通过计算说明Qc=($\frac{1}{2}$×0.01)×($\frac{1}{2}$×0.001)3=6.25×10-13>Ksp=2.097×l0-39,则生成沉淀.
分析 图中D、E、Z是单质,其余均是化合物.且知E为日常常用金属;D元素的原子最外层电子数与电子层数相等,C+D=E+F是置换反应,推断高温下为铝热反应,推断D为Al,E为Fe,F为Al2O3;Z、Y是氯碱工业的产品,由图中Al、Al2O3和Y反应可推断,Y为NaOH;得到Z为Cl2,X为HCl,反应均在水溶液中进行,所以推断得到G为NaAlO2,M为AlCl3,B为FeCl2,A为FeCl3,然后结合物质的性质及化学反应原理来解答.
解答 解:图中D、E、Z是单质,其余均是化合物.且知E为日常常用金属;D元素的原子最外层电子数与电子层数相等,C+D=E+F是置换反应,推断高温下为铝热反应,推断D为Al,E为Fe,F为Al2O3;Z、Y是氯碱工业的产品,由图中Al、Al2O3和Y反应可推断,Y为NaOH;得到Z为Cl2,X为HCl,反应均在水溶液中进行,所以推断得到G为NaAlO2,M为AlCl3,B为FeCl2,A为FeCl3,
(1)X为HCl,其电子式为 ,
,
故答案为: ;
;
(2)pH=12的NaAlO2溶液中,水解显碱性,溶质的阳离子与溶质的阴离子浓度之差为0.01mol/L-10-12mol/L=(10-2-10-12)mol/L,
故答案为:(10-2-10-12)mol/L;
(3)E作为待镀金属,铜为镀层金属,则铜为阳极失去电子,E为阴极,电极反应为Cu2++2e-=Cu,
故答案为:阳;Cu2++2e-=Cu;
(4)反应③中D为Al与Y为 NaOH的水溶液,反应生成偏铝酸钠和氢气,反应的离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑,
故答案为:2Al+2OH-+2H2O=2AlO2-+3H2↑;
(5)Y中滴加M,先没有沉淀后生成沉淀,而M中滴加Y,先生成沉淀后沉淀消失,则试剂互滴现象不同,可以鉴别,
故答案为:Y中滴加M,先没有沉淀后生成沉淀,而M中滴加Y,先生成沉淀后沉淀消失,则Y为NaOH,M为AlCl3;
(6)0.01mol•L-1的FeCl3溶液与0.001mol•L-1的NaOH溶液等体积混合,Qc=($\frac{1}{2}$×0.01)×($\frac{1}{2}$×0.001)3=6.25×10-13>Ksp=2.097×l0-39,则生成沉淀,
故答案为:能;Qc=($\frac{1}{2}$×0.01)×($\frac{1}{2}$×0.001)3=6.25×10-13>Ksp=2.097×l0-39,则生成沉淀.
点评 本题考查无机物的推断,为高频考点,把握物质的性质及转化关系推断物质为解答的关键,涉及盐类水解、电化学反应原理、沉淀的生成等,综合性较强,题目难度中等.

 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案| A. | 红棕色的NO2加压后颜色先变深后变浅(已知:2NO2 (g)?N2O4 (g)) | |
| B. | 实验室中常用排饱和食盐水的方法收集氯气 | |
| C. | 对H2(g)+I2(g)?2HI(g),平衡体系增大压强可使颜色变深 | |
| D. | 工业上生产硫酸的过程中使用过量的空气以提高二氧化硫的利用率 |
| A. | Na | B. | Mg | C. | Cl | D. | Ne |
| A. | c(OH-)>c(H+) | B. | c(NH4+)>c(NH3•H2O) | ||
| C. | c(NH4+)>c(H+)=c(OH-)>c(Cl-) | D. | c(Cl-)>c(NH4+)>c(OH-)>c(H+) |
 A、B、C、D、E为原子序数依次增大的五种短周期元素,其中仅含有一种金属元素,A和D最外层电子数相同;B、C和E在周期表中相邻,且C、E同主族.B、C的最外层电子数之和等于D的原子核外电子数,A和C可形成两种常见的液态化合物.
A、B、C、D、E为原子序数依次增大的五种短周期元素,其中仅含有一种金属元素,A和D最外层电子数相同;B、C和E在周期表中相邻,且C、E同主族.B、C的最外层电子数之和等于D的原子核外电子数,A和C可形成两种常见的液态化合物.