题目内容
铁盐、亚铁盐在工农业生产、生活、污水处理等方面有着极其广泛的应用。
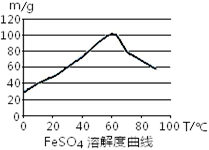
(1)用铁屑与稀硫酸反应制备FeSO4
①制备原理用离子方程式表示为 。若要提高FeSO4生成速率,采取下列措施中正确的是 。
A.使用浓硫酸与铁屑反应
B.使用磨细的铁粉反应
C.控制温度在50~70℃
D.控制温度在80~100℃
②在上述反应过程中,常会伴随发生反应:4Fe2++O2+4H+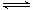 4Fe3++2H2O
4Fe3++2H2O
若要减少产品FeSO4中Fe3+的含量,采取下列措施中正确的是 。
A.控制稀硫酸的浓度不能太高
B.用去O2蒸馏水注入浓硫酸配制反应所需的稀硫酸
C.反应中保持n(Fe)/n(H2SO4) >1
D.反应中应经常添加Fe2(SO4)3搅拌
③反应结束后,将溶液进行 、冷却、过滤、洗涤即得FeSO4·7H2O晶体。
(2)工业上用含有少量Cu、Al的废铁屑制备Fe2(SO4)3
其反应及操作流程如下:
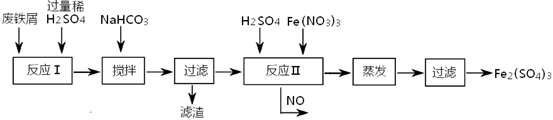
①加入NaHCO3并搅拌,将混合液pH调控至 范围内,使杂质沉淀过滤除去。
②反应Ⅱ中反应的离子方程式是: 。
③生产中,将反应Ⅱ产生的NO配比一种气体X,混合后重新通入反应Ⅱ中,该设计的目的是 ,气体X与NO配比的比例是 。
(3)用Fe2(SO4)3处理含S2-污水时,有黑色沉淀及淡黄色悬浮物产生,其反应的离子方程式是 。

(1)用铁屑与稀硫酸反应制备FeSO4
①制备原理用离子方程式表示为 。若要提高FeSO4生成速率,采取下列措施中正确的是 。
A.使用浓硫酸与铁屑反应
B.使用磨细的铁粉反应
C.控制温度在50~70℃
D.控制温度在80~100℃
②在上述反应过程中,常会伴随发生反应:4Fe2++O2+4H+
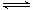 4Fe3++2H2O
4Fe3++2H2O 若要减少产品FeSO4中Fe3+的含量,采取下列措施中正确的是 。
A.控制稀硫酸的浓度不能太高
B.用去O2蒸馏水注入浓硫酸配制反应所需的稀硫酸
C.反应中保持n(Fe)/n(H2SO4) >1
D.反应中应经常添加Fe2(SO4)3搅拌
③反应结束后,将溶液进行 、冷却、过滤、洗涤即得FeSO4·7H2O晶体。
(2)工业上用含有少量Cu、Al的废铁屑制备Fe2(SO4)3
其反应及操作流程如下:

①加入NaHCO3并搅拌,将混合液pH调控至 范围内,使杂质沉淀过滤除去。
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 | Cu(OH)2 |
| 开始沉淀 | 2.3 | 7.5 | 3.4 | 4.7 |
| 完全沉淀 | 3.2 | 9.7 | 4.4 | 6.7 |
②反应Ⅱ中反应的离子方程式是: 。
③生产中,将反应Ⅱ产生的NO配比一种气体X,混合后重新通入反应Ⅱ中,该设计的目的是 ,气体X与NO配比的比例是 。
(3)用Fe2(SO4)3处理含S2-污水时,有黑色沉淀及淡黄色悬浮物产生,其反应的离子方程式是 。
(1)① Fe+2H+=Fe2++H2↑ B、C ② A、C ③ 过滤 (2)① 6.7~7.5
② 3Fe2++NO3-+4H+ =3Fe3++NO↑+2H2O ③ 节约Fe(NO3)3、防止NO污染 3 : 4
(3)2Fe3++3S2- ="2" FeS↓+S
② 3Fe2++NO3-+4H+ =3Fe3++NO↑+2H2O ③ 节约Fe(NO3)3、防止NO污染 3 : 4
(3)2Fe3++3S2- ="2" FeS↓+S
试题分析:(1)铁和氢离子发生置换反应制备硫酸亚铁,可以使用铁粉增大接触面积,加快速率,B正确;但是不能用浓硫酸,铁在常温条件下遇浓硫酸钝化,A错误;硫酸亚铁在60℃时溶解度高,所以选择温度在50~70℃,C正确,D错误。减少Fe2+被氧化,控制硫酸浓度,减少H+浓度,平衡逆向移动,A正确,B、稀释浓硫酸应该把硫酸向水中加,并不断搅拌,错误;C、铁过量可以防止Fe2+被氧化,正确;D、加入Fe3+将会增加Fe3+浓度,错误。反应结束后,过滤除去过量的铁,再降低温度,硫酸亚铁的溶解度减小,析出晶体。(2)废铁屑加入过量的稀硫酸,铁和铝溶解,铜不溶,再加NaHCO3调PH至6.7~7.5之间,Al3+、Cu2+沉淀,再过滤,加入氧化剂把Fe2+氧化,蒸发结晶得产物。为了节约Fe(NO3)3、防止NO污染,可以利用氧气和NO按照3:4反应生成硝酸做氧化剂。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目