题目内容
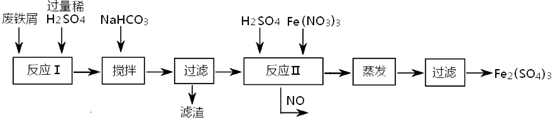
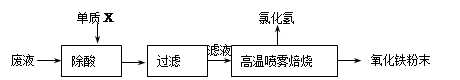
绿矾(FeSO4·7H2O)是治疗缺铁性贫血药品的重要成分。下面是以市售铁屑(含少量锡、氧化铁等杂质)为原料生产纯净绿矾的一种方法:

查询资料,得有关物质的数据如下表:
(1)检验制得的绿矾晶体中是否含有Fe3+,最好选用的试剂为 。
A.KSCN溶液 B.NaOH溶液 C.KMnO4溶液 D.苯酚溶液
(2)操作II中,通入硫化氢至饱和的目的是 ;在溶液中用硫酸酸化至pH=2的目的是 。
(3)操作IV的顺序依次为 、冷却结晶、 。
(4)操作IV得到的绿矾晶体用少量冰水洗涤,其目的是:①除去晶体表面附着的硫酸等杂质;② 。
(5)测定绿矾产品中Fe2+含量的方法是:a.称取2.850g绿矾产品,溶解,在250mL容量瓶中定容;b.量取25.00mL待测溶液于锥形瓶中;c.用硫酸酸化的0.01000mol/LKMnO4溶液滴定至终点,消耗KMnO4溶液体积的平均值为20.00mL。
①滴定时盛放KMnO4溶液的仪器为 (填仪器名称)。
②判断此滴定实验达到终点的方法是 。
③计算上述样品中FeSO4·7H2O的质量分数为 。

查询资料,得有关物质的数据如下表:
| 25℃时 | pH值 |
| 饱和H2S溶液 | 3.9 |
| SnS沉淀完全 | 1.6 |
| FeS开始沉淀 | 3.0 |
| FeS沉淀完全 | 5.5 |
(1)检验制得的绿矾晶体中是否含有Fe3+,最好选用的试剂为 。
A.KSCN溶液 B.NaOH溶液 C.KMnO4溶液 D.苯酚溶液
(2)操作II中,通入硫化氢至饱和的目的是 ;在溶液中用硫酸酸化至pH=2的目的是 。
(3)操作IV的顺序依次为 、冷却结晶、 。
(4)操作IV得到的绿矾晶体用少量冰水洗涤,其目的是:①除去晶体表面附着的硫酸等杂质;② 。
(5)测定绿矾产品中Fe2+含量的方法是:a.称取2.850g绿矾产品,溶解,在250mL容量瓶中定容;b.量取25.00mL待测溶液于锥形瓶中;c.用硫酸酸化的0.01000mol/LKMnO4溶液滴定至终点,消耗KMnO4溶液体积的平均值为20.00mL。
①滴定时盛放KMnO4溶液的仪器为 (填仪器名称)。
②判断此滴定实验达到终点的方法是 。
③计算上述样品中FeSO4·7H2O的质量分数为 。
(1)AD
(2)除去溶液中的Sn2+离子,并防止Fe2+被氧化;防止Fe2+离子生成沉淀
(3)蒸发浓缩;过滤洗涤
(4)降低洗涤过程中FeSO4·7H2O的损耗
(5)①酸式滴定管
②滴加最后一滴KMnO4溶液时,溶液变成浅红色且半分钟内不褪色。
③0.975
试题分析:(1)检验Fe3+通常用KSCN溶液,加入KSCN溶液,溶液显血红色;Fe3+加入苯酚溶液,溶液显紫色,据此也可检验Fe3+。
(2)通入H2S可以使Sn2+完全沉淀,S2-具有还原性,还可以防止Fe2+被氧化。根据题中数据,将溶液酸化至pH=2,目的是只沉淀Sn2+,防止Fe2+沉淀。
(3)从溶液中得到晶体的操作一般为蒸发浓缩、冷却结晶、过滤洗涤。
(4)用冰水洗涤一方面可以出去杂质,另一方面降低FeSO4·7H2O的溶解度,减小洗涤过程中的损失。
(5)①盛放酸性高锰酸钾溶液应用酸式滴定管。
②高锰酸钾溶液有颜色,滴入最后一滴时,溶液显浅红色,且半分钟不褪色,则达到终点。
③根据关系式5Fe2+~KMnO4,可知样品中所含FeSO4·7H2O的物质的量为0.01000mol/L×0.02L×5×10=0.01mol,故样品中FeSO4·7H2O的质量分数为
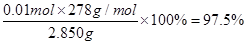 。
。
练习册系列答案
相关题目
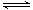 4Fe3++2H2O
4Fe3++2H2O