题目内容
11.亚氯酸钠(NaClO2)是一种强氧化性漂白剂,广泛用于纺织、印染和食品工业.它在碱性环境中稳定存在.某同学查阅资料后设计生产NaClO2的主要流程如下.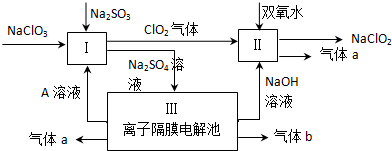
(1)Ⅰ、Ⅲ中发生反应的还原剂分别是Na2SO3、H2O(填化学式).
(2)Ⅱ中反应的离子方程式是2ClO2+H2O2+2OH-=2ClO2-+O2↑+2H2O.
(3)A的化学式是H2SO4,装置Ⅲ中A在阳极区产生.
(4)ClO2是一种高效水处理剂,可用亚氯酸钠和稀盐酸为原料制备.写出该制备反应的化学方程式5NaClO2+4HCl=5NaCl+4ClO2↑+2H2O.
(5)NaClO2变质可分解为NaClO3和NaCl,取等质量变质前后的NaClO2试样均配成溶液,分别与足量FeSO4溶液反应时,消耗Fe2+的物质的量相同.(填“相同”,“不同”或“无法判断”)
分析 硫酸钠溶液通入离子隔膜电解池中,ClO2和双氧水在II中发生氧化还原反应生成NaClO2和气体a,该反应中Cl元素化合价由+4价变为+3价,则O元素化合价由-1价变为0价,所以生成的气体a是O2,离子反应方程式为2 ClO2+H2O2+2OH-=2 ClO2-+O2↑+2H2O;
III中发生电解,根据图知,生成氢氧化钠,阴极上生成氢气同时阴极附近生成NaOH,所以生成的气体b是H2;阳极上氢氧根离子放电生成氧气,所以a是O2,同时生成硫酸,所以A溶液是硫酸;酸性条件下,I中NaClO2、Na2SO3发生氧化还原反应,离子反应方程式为2ClO3-+2H++SO32-=2ClO2↑+SO42-+H2O;
(1)同一化学反应中,失电子化合价降低的反应物是还原剂;
(2)碱性条件下,ClO2、H2O2发生氧化还原反应生成氧气、ClO2-和水;
(3)通过以上分析知,A是硫酸,硫酸在阳极附近生成;
(4)亚氯酸钠和稀盐酸反应生成ClO2和NaCl、水;
(5)已变质和未变质的NaClO2与Fe2+反应都生成Cl-,根据转移电子守恒判断.
解答 解:硫酸钠溶液通入离子隔膜电解池中,ClO2和双氧水在II中发生氧化还原反应生成NaClO2和气体a,该反应中Cl元素化合价由+4价变为+3价,则O元素化合价由-1价变为0价,所以生成的气体a是O2,离子反应方程式为2 ClO2+H2O2+2OH-=2 ClO2-+O2↑+2H2O;
III中发生电解,根据图知,生成氢氧化钠,阴极上生成氢气同时阴极附近生成NaOH,所以生成的气体b是H2;阳极上氢氧根离子放电生成氧气,所以a是O2,同时生成硫酸,所以A溶液是硫酸;酸性条件下,I中NaClO2、Na2SO3发生氧化还原反应,离子反应方程式为2ClO3-+2H++SO32-=2ClO2↑+SO42-+H2O;
(1)同一化学反应中,失电子化合价降低的反应物是还原剂,
I中反应方程式为2ClO3-+2H++SO32-=2ClO2↑+SO42-+H2O,还原剂是Na2SO3;III中氧化剂和还原剂都是水,故答案为:Na2SO3;H2O;
(2)碱性条件下,ClO2、H2O2发生氧化还原反应生成氧气、ClO2-和水,离子方程式为2ClO2+H2O2+2OH-=2ClO2-+O2↑+2H2O,
故答案为:2ClO2+H2O2+2OH-=2ClO2-+O2↑+2H2O;
(3)通过以上分析知,电解硫酸钠溶液,阳极上氢氧根离子放电生成氧气,同时生成硫酸,所以A是硫酸,硫酸在阳极附近生成,故答案为:硫酸;阳;
(4)亚氯酸钠和稀盐酸反应生成ClO2和NaCl、水,反应方程式为5NaClO2+4HCl=5NaCl+4ClO2↑+2H2O,故答案为:5NaClO2+4HCl=5NaCl+4ClO2↑+2H2O;
(5)Fe2+与变质前后的NaClO2反应,最后的还原产物都是NaCl,根据电子守恒消耗的Fe2+物质的量应相同,故答案为:相同.
点评 本题考查制备实验方案设计,为高频考点,明确I、II、III中发生的反应及物质的性质是解本题关键,熟悉常见物质的性质,难点是离子方程式的书写.

 阅读快车系列答案
阅读快车系列答案| A. | N(Ne)>N(H2)>N(O2) | B. | N(O2)>N(Ne)>N(H2) | C. | N(H2)>N(O2)>N(Ne) | D. | N(H2)>N(Ne)>N(O2) |
| A. | CuSO4 •5H2O 是混合物 | |
| B. | 含Fe元素质量分数为70%的Fe2O3是纯净物 | |
| C. | 冰和水混合在一起形成混合物 | |
| D. | 由单质形成的物质一定是纯净物 |



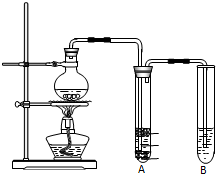
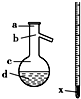 实验室中用苯甲醛制备苯甲醇和苯甲酸,已知反应原理:2HCHO+KOH-→CH3OH+HCOOK
实验室中用苯甲醛制备苯甲醇和苯甲酸,已知反应原理:2HCHO+KOH-→CH3OH+HCOOK
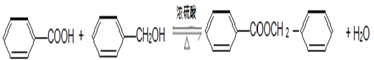 ,实验室在收集此特殊香味的物质时常用饱和Na2CO3溶液 (填试剂名称)除去其中的杂质,且便于其分层析出.
,实验室在收集此特殊香味的物质时常用饱和Na2CO3溶液 (填试剂名称)除去其中的杂质,且便于其分层析出.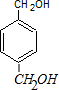 .
.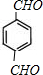 +2H2O.
+2H2O.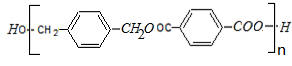 +2nNaOH$→_{△}^{NaOH溶液}$n
+2nNaOH$→_{△}^{NaOH溶液}$n +n
+n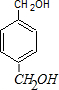 .
.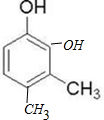 (或
(或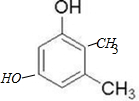 等)(只写出一种即可).
等)(只写出一种即可).