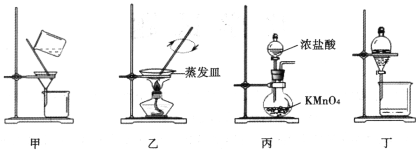
题目内容
【题目】现有短周期元素A、B、C、D。A元素M层上有2对成对电子,D与A在周期表中同一主族。由A、B与D组成的化合物的浓溶液是常见的干燥剂,常温下C单质为双原子分子,其氢化物水溶液呈碱性,是一种重要肥料。
(1)A的原子最外层共有___种不同运动状态的电子,该原子共有___种不同能量的电子,能量最高的电子占有___个轨道,其电子云形状为____。
(2)元素A、B与D组成的化合物的浓溶液是常见干燥剂,该化合物在实验室制备乙酸乙酯时所起的作用:_____。
(3)B与C元素形成带一个单位正电荷的离子,写出该微粒的电子式____。
(4)元素A与元素D相比,非金属性较强的是____(用元素符号表示),下列表述中能表明这一事实的是____。
①比较最高价氧化物对应水化物的酸性
②比较对应气态氢化物的稳定性
③一定条件下D能从A的氢化物水溶液中置换出A单质
④A单质的熔沸点明显高于D单质
从原子结构分析A和D非金属强弱的原因_____。
(5)C原子的原子结构示意图:_____,C的氢化物固态时属于____晶体。
【答案】6 5 3 哑铃形 催化剂、吸水剂 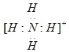 O ②③ 硫原子和氧原子最外层电子数相同,但硫原子比氧原子多一个电子层,半径较大,对外层电子的吸引力弱,故非金属性较弱
O ②③ 硫原子和氧原子最外层电子数相同,但硫原子比氧原子多一个电子层,半径较大,对外层电子的吸引力弱,故非金属性较弱 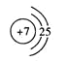 分子
分子
【解析】
现有短周期元素A、B、C、D,A元素M层上有2对成对电子,A的M层含有6个电子,为S元素;D与A在周期表中同一主族,则D为O元素;由A、B与D组成的化合物的浓溶液是常见的干燥剂,该干燥剂为浓硫酸,则B为H元素;常温下C单质为双原子分子,其氢化物水溶液呈碱性,是一种重要的肥料,则C为N元素。
(1)A为S原子,其最外层含有6个电子,则最外层共有6种不同运动状态的电子;S有1s、2s、2p、3s、3p共有5种不同能量的电子,能量最高的电子在3p能级,占有3个轨道,其电子云形状为哑铃形。
(2)元素A、B与D组成的化合物的浓溶液是常见干燥剂,该干燥剂为浓H2SO4,该化合物在实验室制备乙酸乙酯时所起的作用:催化剂、吸水剂;。
(3)B与C元素形成带一个单位正电荷的离子为铵根离子,铵根离子是阳离子,电子式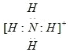 。
。
(4)元素A与元素D相比,即元素S与元素O相比,位于同一主族,原子序数越大,非金属性越弱,非金属性较强的是O;
①比较最高价氧化物对应水化物的酸性,但O元素没有含氧酸,无法据此判断非金属性强弱,故①错误;
②比较对应气态氢化物的稳定性,氢化物稳定性越强,非金属性越强,通过比较对应气态氢化物的稳定性,可以判断二者非金属性强弱,故②正确;
③一定条件下氧气能从硫化氢的水溶液中置换出S单质,证明O的非金属性大于S,故③正确;
④沸点大小与非金属性没有必然关系,无法根据沸点高低判断非金属性强弱,故④错误;
故选②③;
A和D非金属强弱的原因:硫原子和氧原子最外层电子数相同,但硫原子比氧原子多一个电子层,半径较大,对外层电子的吸引力弱,故非金属性较弱;
(5)N原子的原子结构示意图: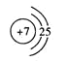 ,C为N元素,其氢化物为氨气,氨气在固态时属于分子晶体。
,C为N元素,其氢化物为氨气,氨气在固态时属于分子晶体。