题目内容
【题目】为探究黑色固体X(仅含两种元素)的组成和性质,设计并完成如下实验: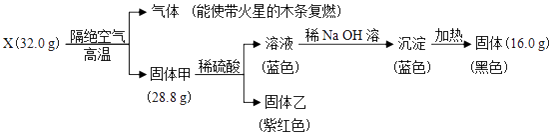
请回答:
(1)X的化学式是 .
(2)固体甲与稀硫酸反应的离子方程式是 .
(3)加热条件下氨气被固体X氧化成一种气体单质,写出该反应的化学方程式 .
【答案】
(1)CuO
(2)Cu2O+2H+=Cu++Cu+H2O
(3)3CuO+2NH3 ![]() 3Cu+N2+3H2O
3Cu+N2+3H2O
【解析】解:流程中32gX隔绝空气加热分解放出了能使带火星的木条复燃的气体为氧气,质量=32.0g﹣28.8g=3.28g,证明X中含氧元素,28.8g固体甲和稀硫酸溶液反应生成蓝色溶液,说明含铜离子,证明固体甲中含铜元素,即X中含铜元素,铜元素和氧元素形成的黑色固体为CuO,X为氧化铜,n(CuO)= ![]() =0.4mol,结合质量守恒得到n(O2)=
=0.4mol,结合质量守恒得到n(O2)= ![]() =0.1mol,氧元素守恒得到甲中n(Cu):n(O)=0.2mol:(0.4mol﹣0.1mol×2)=2:1,固体甲化学式为Cu2O,固体乙为Cu,蓝色溶液为硫酸铜,加入氢氧化钠溶液生成氢氧化铜沉淀,加热分解得到16.0g氧化铜,(1)分析可知X为CuO,所以答案是:CuO;(2)固体甲为Cu2O,氧化亚铜和稀硫酸溶液反应发生气化反应生成铜、亚铜离子,反应的离子方程式为:Cu2O+2H+=Cu++Cu+H2O,
=0.1mol,氧元素守恒得到甲中n(Cu):n(O)=0.2mol:(0.4mol﹣0.1mol×2)=2:1,固体甲化学式为Cu2O,固体乙为Cu,蓝色溶液为硫酸铜,加入氢氧化钠溶液生成氢氧化铜沉淀,加热分解得到16.0g氧化铜,(1)分析可知X为CuO,所以答案是:CuO;(2)固体甲为Cu2O,氧化亚铜和稀硫酸溶液反应发生气化反应生成铜、亚铜离子,反应的离子方程式为:Cu2O+2H+=Cu++Cu+H2O,
所以答案是:Cu2O+2H+=Cu++Cu+H2O;(3)加热条件下氨气被固体X位氧化铜氧化成一种气体单质为氮气,反应的化学方程式为:3CuO+2NH3 ![]() 3Cu+N2+3H2O,
3Cu+N2+3H2O,
所以答案是:3CuO+2NH3 ![]() 3Cu+N2+3H2O.
3Cu+N2+3H2O.

练习册系列答案
相关题目