题目内容
【题目】W、X、Y、Z是四种常见的短周期元素其原子半径随原子序数的变化如下图。
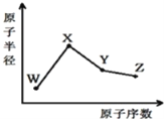
已知W一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的非金属性在同周期中最强。下列说法正确的是 ( )
A. 对应的气态氢化物的稳定性:Y>Z
B. X的非金属性是同周期中最强的
C. 对应简单离子的半径:X>W
D. Y的氧化物能与X的最高价氧化物对应的水化物反应
【答案】D
【解析】W、X、Y、Z是四种常见的短周期元素,已知W的一种核素的质量数为18,中子数为10,则W元素原子的质子数为18-10=8,故W为氧元素;X和Ne原子的核外电子数相差1,X为Na或F,X原子半径大于氧原子,故X为Na元素;Y的单质是一种常见的半导体材料,原子序数大于Na元素,故Y为Si元素;Z的非金属性在同周期元素中最强,故Z为Cl元素,则A.非金属性Cl>Si,故氢化物稳定性Y<Z,A错误;B.Na的金属性是同周期中最强的,B错误;C.电子层结构相同核电荷数越大离子半径越小,故离子半径O2->Na+,C错误;D.二氧化硅能与氢氧化钠反应生成硅酸钠与水,D正确,答案选D。

【题目】Ⅰ.由A、B、C、D四种金属按下表中装置进行实验。
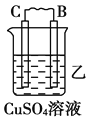
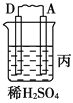
装置 |
|
|
|
现象 | 二价金属A不断溶解 | C的质量增加 | A上有气体产生 |
根据实验现象回答下列问题:
(1)装置甲中负极的电极反应式是_______________,装置乙中正极的电极反应式是___________。
(2)四种金属活泼性由强到弱的顺序是_____________________________________。
Ⅱ.美国阿波罗宇宙飞船上使用了一种新型发电装置—氢氧燃料电池,其构造如图所示,其中a、b两个电极均由多孔的碳炔组成,该电池的负极反应式为_________________,若该电池工作时溶液中增加1molH2O,则理论上电路中通过电子的物质的量为________mol。