题目内容
19.已知短周期元素的离子:aA2+、bB+、cC3-、dD-都具有相同的电子层结构,则下列叙述正确的是( )| A. | 原子半径 A>B>D>C | B. | 原子序数 d>c>b>a | ||
| C. | 离子半径 C>D>B>A | D. | 单质的还原性 A>B>D>C |
分析 已知短周期元素的离子,aA2+、bB+、cC3-、dD- 都具有相同的电子层结构,则离子核外电子数相同,即a-2=b-1=c+3=d-1,原子序数A>B>D>C,A、B处于同一周期,C、D处于同一周期,且A、B处于C、D所在周期的相邻下一周期,A、B形成阳离子,则A、B为金属,C、D形成阴离子,则C、D为非金属,结合元素周期律进行解答.
解答 解:已知短周期元素的离子,aA2+、bB+、cC3-、dD- 都具有相同的电子层结构,则离子核外电子数相同,即a-2=b-1=c+3=d-1,原子序数A>B>D>C,A、B处于同一周期,C、D处于同一周期,且A、B处于C、D所在周期的相邻下一周期,A、B形成阳离子,则A、B为金属,C、D形成阴离子,则C、D为非金属.
A.A、B处于同一周期,C、D处于同一周期,且A、B处于C、D所在周期的相邻下一周期,同周期,原子序数越大原子半径越小,所以原子半径B>A,C>D,电子层越大原子半径越大,所以原子半径B>A>C>D,故A错误;
B.aA2+、bB+、cC3-、dD- 都具有相同的电子层结构,则离子核外电子数相同,即a-2=b-1=c+3=d-1,原子序数a>b>d>c,故B错误;
C.电子层结构相同,核电荷数越大,离子半径越小,核电荷数A>B>D>C,所以离子半径:C3->D->B+>A2+,故C正确;
D.A、B处于同一周期,A、B形成阳离子,则A、B为金属,原子序数A>B,单质还原性B>A,C、D处于同一周期,C、D形成阴离子,则C、D为非金属,原子序数D>C,单质氧化性D>C,故D错误.
故选C.
点评 本题考查位置结构性质的相互关系及应用,根据核外电子排布确定元素所在周期表中的位置以及把握元素周期律的递变规律是解答该题的关键,也可以确定具体的元素进行解答,题目难度不大.

 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案| A. | 2 CH4 (g)+4O2(g)=2CO2(g)+4H2O(l)△H=+890kJ/mol | |
| B. | CH4+2 O2=CO2+2H2O△H=-890kJ/mol | |
| C. | CH4 (g)+2O2(g)=CO2(g)+2H2O(l)△H=-890kJ/mol | |
| D. | $\frac{1}{2}$CH4 (g)+O2(g)=$\frac{1}{2}$CO2(g)+H2O(g)△H=-445kJ/mol |
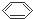 -OH)2用它制成的试纸可以检验溶液的酸碱性.能够跟1mol该化合物起反应的Br2水溶液或H2的最大用量分别是( )
-OH)2用它制成的试纸可以检验溶液的酸碱性.能够跟1mol该化合物起反应的Br2水溶液或H2的最大用量分别是( )| A. | 3 mol 3 mol | B. | 3 mol 5 mol | C. | 6 mol 6 mol | D. | 6 mol 10 mol |
| A. | c(Z)=0.45mol/L | B. | c(Y2)=0.5mol/L | C. | c(X2)=0 | D. | c(X2)=0.5mol/L |
 如图表示元素周期表前四周期的一部分,关于元素X、Y、Z、W的叙述正确的是( )
如图表示元素周期表前四周期的一部分,关于元素X、Y、Z、W的叙述正确的是( )①X、Y的氧化物对应的水化物的酸性为Y<X
②W的原子序数比Z的大9
③W的单质常温下呈液态,可与铁粉反应
④Y、Z的气态氢化物的稳定性Y<Z.
| A. | ①③ | B. | ①② | C. | ②③ | D. | ③④ |
| A. | 漂粉精 | B. | 冰醋酸 | C. | 汽油 | D. | 铝热剂 |
| 元素编号 元素性质 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
| 原子半径/10-10 m | 0.66 | 1.36 | 1.23 | 1.10 | 0.99 | 1.54 | 0.70 | 1.18 |
| 最高或最低化合价 | +2 | +1 | +5 | +7 | +1 | +5 | +3 | |
| -2 | -3 | -1 | -3 |
| A. | 最高价氧化物的水化物酸性:④>⑤ | B. | 与水反应的剧烈程度:②>⑥ | ||
| C. | 气态氢化物的稳定性:④>⑦ | D. | ①⑥⑦形成的化合物是离子化合物 |

 .
.