题目内容
【题目】工业上常用电解对含氮生活污水进行处理。若污水中含有Cl-,主要靠有效氯(HC1O、ClO-)将NH4+氧化为N2。其工作原理如图所示,下列分析正确的是
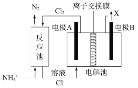
A.电极A为阴极
B.电极B上发生电极反应:2H++2e-=H2↑
C.电解池中离子交换膜为阴离子交换膜
D.处理含l mol NH4+的废水,反应池中共转移电子数目为3NA
【答案】B
【解析】
A. 根据装置图可知在电极A上,溶液中的Cl-失去电子变为Cl2,所以A电极为阳极,A错误;
B. 根据选项A分析可知:电极A为阳极,电极B为阴极,溶液中的H+得到电子变为H2,电极反应式为:2H++2e-=H2↑,B正确;
C. 电解池中H+不断放电,使电解池的阴极阳离子浓度降低,为了维持平衡,左侧的阳离子要通过离子交换膜进入右侧,所以离子交换膜为阳离子交换膜,C错误;
D. 处理含l mol NH4+的废水,N元素化合价由-3价变为N2的0价,转移3 mol电子,在电解池中反应产生Cl2时也要转移3 mol电子,右侧反应池中共转移电子数目为3NA,故反应池中共转移电子数目为6NA,D错误;
故合理选项是B。

【题目】在100℃时,将0.40 mol二氧化氮气体充入一个2 L抽空的密闭容器中,发生反应:2NO2 N2O4。每隔一段时间就对该容器内的物质进行分析,得到下表数据:
时间/s | 0 | 20 | 40 | 60 | 80 |
n(NO2)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
n(N2O4)/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
(1)在上述条件下,从反应开始至20 s时,用NO2表示的平均反应速率为__________mol·L1·s1。
(2)n3________(填“>”“<”或“=”)n4;该反应的平衡常数K的数值为___________(精确到0.1)。
(3)若在相同条件下最初向该容器中充入N2O4,要达到上述平衡状态,N2O4的起始浓度是______mol·L1。
(4)上述(3)达到平衡后N2O4的转化率为______________,混合气体的平均摩尔质量为______________。
(5)达到平衡后,如果升高温度,气体颜色会变深,则升高温度后,反应2NO2N2O4的平衡常数将_______________(填“增大”“减小”或“不变”)。
(6)达到平衡后,如果向该密闭容器中再充入0.32 mol He,并把容器体积扩大为4 L,则平衡将______________(填“向左移动”“向右移动”或“不移动”)。
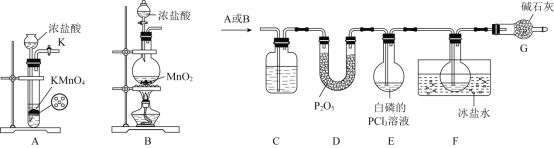
【题目】ClO2作为一种广谱型的消毒剂,将逐渐用来取代Cl2成为自来水的消毒剂。已知ClO2是一种易溶于水而难溶于有机溶剂的气体,11℃时液化成红棕色液体。
(1)某研究小组用下图装置制备少量ClO2(夹持装置已略去)。
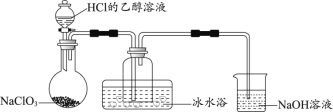
①冰水浴的作用是____________。
②NaOH溶液的主要作用为吸收反应产生的Cl2,其吸收液可用于制取漂白液,该吸收反应的氧化剂与还原剂之比为___________________。
③以NaClO3和HCl为原料制备ClO2的化学方程式为_________________________。
(2)将ClO2水溶液滴加到KI溶液中,溶液变棕黄;再向其中加入适量CCl4,振荡、静置,观察到________,证明ClO2具有氧化性。
(3)ClO2在杀菌消毒过程中会产生Cl-,其含量一般控制在0.3-0.5 mg·L1,某研究小组用下列实验方案测定长期不放水的自来水管中Cl-的含量:量取10.00 mL的自来水于锥形瓶中,以K2CrO4为指示剂,用0.0001mol·L-1的AgNO3标准溶液滴定至终点。重复上述操作三次,测得数据如下表所示:
实验序号 | 1 | 2 | 3 | 4 |
消耗AgNO3溶液的体积/mL | 10.24 | 10.02 | 9.98 | 10.00 |
①在滴定管中装入AgNO3标准溶液的前一步,应进行的操作_____________。
②测得自来水中Cl-的含量为______ mg·L1。
③若在滴定终点读取滴定管刻度时,俯视标准液液面,则测定结果_______(填“偏高”、“偏低”或“无影响”)。
【题目】根据要求完成下列各小题:
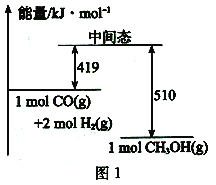
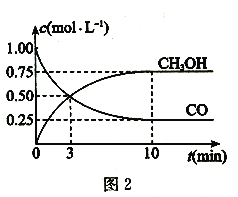
Ⅰ.(1)理论上稀的强酸、强碱反应生成1mol H2O(l)时放出57.3kJ的热量,写出表示稀硫酸和稀氢氧化钠溶液反应的中和热的热化学方程式________ 。
(2)已知:乙苯催化脱氢制苯乙烯反应:苯在计算键能时,此处可看作为![]() ,
, ![]()
![]()
![]() +H2(g)
+H2(g)
化学键 | C—H | C—C | C=C | H—H |
键能/kJ·mol-1 | 412 | 348 | 612 | 436 |
计算上述反应的ΔH=________ kJ·mol-1。
Ⅱ.25 ℃时,部分物质的电离平衡常数如表所示,请回答下列问题:
化学式 | CH3COOH | H2CO3 | HClO |
电离平衡常数 | 1.7×10-5 | K1=4.3×10-7 K2=5.6×10-11 | 3.0×10-8 |
(1)CH3COOH、H2CO3、HClO的酸性由强到弱的顺序为_______。
(2)将少量CO2气体通入NaClO溶液中,写出反应的离子方程式:________。