题目内容
13.化学已渗透到人类生活的各个方面.下列说法正确的是( )| A. | 为防止富脂食品氧化变质,常在包装袋中放入生石灰 | |
| B. | 铬是人体必需的微量元素,但铬过量会危害人体健康,其中六价铬的毒性最大.人体内六价铬超标,可以服用维生素C缓解毒性,说明维生素C具有氧化性 | |
| C. | 去年冬天的雾霾天气严重影响了人们的正常出行和生活节奏.为改善空气质量,可以加高工厂的烟囱,使烟尘和废气远离地表 | |
| D. | 硅酸钠是最简单的硅酸盐,是制备硅胶和木材防火剂的原料 |
分析 A、注意氧化还原反应的实质,食品被氧化的实质是被空气中的氧气氧化;
B.维生素C有还原性;
C.加高工厂的烟囱,烟尘和废气仍排入空气中;
D.硅酸钠具有粘性,用来制备硅胶;
解答 解:A、生石灰无还原性不能与氧化性物质反应,故不能防止食品氧化,故A错误;
B.维生素C有还原性,能还原六价铬,故B错误;
C.加高工厂的烟囱,烟尘和废气仍排入空气中,仍会有污染,故C错误;
D.硅酸钠不与氧气反应,易溶于水具有粘性,可用来制备硅胶和木材防火剂的原料,故D正确;
故选D.
点评 本题考查食品添加剂、环境污染等,侧重于化学与人体健康的考查,为高考常见题型和高频考点,有利于培养学生的良好科学素养,难度不大,注意相关基础知识的积累.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
3.制备氢气通常有下列四种方法.a.电解水制氢:2H2O$\frac{\underline{\;电解\;}}{\;}$2H2↑+O2↑
b.高温使水分解制氢:2H2O$\frac{\underline{\;高温\;}}{\;}$2H2↑+O2↑
c.太阳光催化分解水制氢:2H2O$\frac{\underline{\;\;\;TiO_{2}\;\;\;}}{太阳光}$2H2↑+O2↑
d.天然气制氢:CH4+H2O$\frac{\underline{\;高温\;}}{\;}$CO+3H2 下列说法正确的是( )
b.高温使水分解制氢:2H2O$\frac{\underline{\;高温\;}}{\;}$2H2↑+O2↑
c.太阳光催化分解水制氢:2H2O$\frac{\underline{\;\;\;TiO_{2}\;\;\;}}{太阳光}$2H2↑+O2↑
d.天然气制氢:CH4+H2O$\frac{\underline{\;高温\;}}{\;}$CO+3H2 下列说法正确的是( )
| A. | 方法d是最为节能的一种方法 | |
| B. | 方法a~d中,H2O分子中的共价键全部断裂 | |
| C. | H2O、H2O2所含的化学键类型完全相同 | |
| D. | H2O是共价化合物,CH4是离子化合物 |
1.化学中常用图象直观地描述化学反应的进程或结果.只改变一个条件,则下列对图象的解读正确的是( )
| A. | 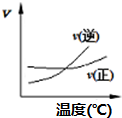 A2(g)+3B2(g)?2AB3(g)如图说明此反应的正反应是吸热反应 | |
| B. | 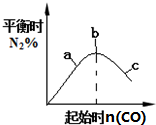 4CO(g)+2NO2(g)?N2(g)+4CO2(g)如图说明NO2的转化率b>a>c | |
| C. |  N2(g)+3H2(g)?2NH3(g)如图说明t秒时合成氨反应达到平衡 | |
| D. |  2A(g)+2B(g)?3C(g)+D(?)如图说明生成物D一定是气体 |
8.在含有0.6molCl-、0.8molSO42-及一定量Mg2+和Al3+的混合溶液中,滴入一定浓度NaOH溶液,产生沉淀情况如图(不考虑Mg2+和Al3+水解及水电离对离子数目的影响).若反应前Al3+的物质的量为a mol,Al3+的物质的量与混合溶液中离子总物质的量的比值为x.则( )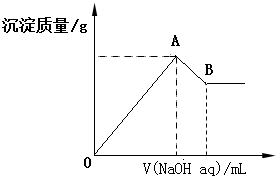

| A. | x=$\frac{2a}{5-a}$ | |
| B. | x的取值范围是0<x<$\frac{11}{32}$ | |
| C. | A点横坐标的值随x发生变化 | |
| D. | 若B点横坐标为200mL时,c(NaOH)=7.0mol/L |
18.下列各表述与下图所示一致的是( )
| A. | 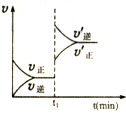 表示某吸热反应t1时刻升高温度时,正逆反应速率的变: | |
| B. | 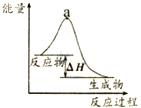 表示某放热反应过程的能量变化,若使用催化剂,a点会降低 | |
| C. | 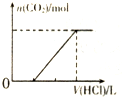 表示向含等物质的量的NaOH、Na2CO3混合溶液中滴加0.1 mol•L-1盐酸至过量时,产生气体的体积与消耗盐酸的关系 | |
| D. | 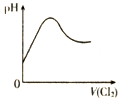 表示Cl2通入H2SO3溶液中pH的变化 |
5.下列说法正确的是( )
| A. | 按系统命名法,有机物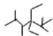 的名称是 2,2,4,5-四甲基-3,3-二乙基己烷 的名称是 2,2,4,5-四甲基-3,3-二乙基己烷 | |
| B. | 苯、甲苯、二甲苯互为同系物,均能使酸性高锰酸钾溶液褪色 | |
| C. | 等质量的苯、乙炔(CH≡CH)、乙烯和甲烷分别在氧气中充分燃烧,所消耗的氧气的量依次增加 | |
| D. | 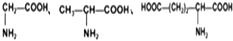 三种氨基酸之间脱水,最多可生成6种二肽 三种氨基酸之间脱水,最多可生成6种二肽 |

 一定温度下,在2L的密闭容器中,X、Y、Z三种气体的量随时间变化的曲线如图所示:
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的量随时间变化的曲线如图所示: