题目内容
2. 一定温度下,在2L的密闭容器中,X、Y、Z三种气体的量随时间变化的曲线如图所示:
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的量随时间变化的曲线如图所示:(1)从反应开始到10s,用Z表示的反应速率0.079mol/(L•s).X的物质的量浓度减少了0.395mol/L,Y的转化率为79%.
(2)该反应的化学方程式为X+Y?2Z.
分析 图象分析可知起始量为:X=1.2mol,Y=1.00mol,Z=1.58mol,10s达到平衡状态xyz的物质的量为:0.41mol,0.21mol,1.58mol
(1)反应速率v=$\frac{△c}{△t}$,浓度c=$\frac{n}{V}$,转化率=$\frac{消耗量}{起始量}$×100%;
(2)反应的化学方程式计量数之比等于物质参加反应的物质的量之比,据此写出化学方程式.
解答 解:图象分析可知起始量为:X=1.2mol,Y=1.00mol,Z=1.58mol,10s达到平衡状态xyz的物质的量为:0.41mol,0.21mol,1.58mol,△X=1.2mol-0.41mol=0.79mol,△Y=1.00mol-0.21mol=0.79mol,△Z=1.58mol
(1)反应速率v(Z)=$\frac{△c}{△t}$=$\frac{\frac{1.58mol}{2L}}{10s}$=0.079mol/(L•s),
X的浓度减小c=$\frac{n}{V}$=$\frac{0.79mol}{2L}$=0.395mol/L,
Y转化率=$\frac{消耗量}{起始量}$×100%=$\frac{0.79mol}{1.00mol}$×100%=79%;
故答案为:0.079mol/(L•s);0.395mol/L;79%;
(2)n(X):n(Y):n(Z)=0.79:0.79:1.58=1:1:2,反应的化学方程式计量数之比等于物质参加反应的物质的量之比,可知化学方程式为:X+Y?2Z,
故答案为:X+Y?2Z.
点评 本题考查了图象分析判断,化学方程式书写方法,反应速率、浓度和转化率的计算应用,掌握基础是关键,题目较简单.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
12. 科学家研制出的八硝基立方烷(结构如图所示,碳原子未画出)是一种新型高能炸药,爆炸分解得到无毒、稳定的物质,下列说法正确的是( )
科学家研制出的八硝基立方烷(结构如图所示,碳原子未画出)是一种新型高能炸药,爆炸分解得到无毒、稳定的物质,下列说法正确的是( )
 科学家研制出的八硝基立方烷(结构如图所示,碳原子未画出)是一种新型高能炸药,爆炸分解得到无毒、稳定的物质,下列说法正确的是( )
科学家研制出的八硝基立方烷(结构如图所示,碳原子未画出)是一种新型高能炸药,爆炸分解得到无毒、稳定的物质,下列说法正确的是( )| A. | 分子中不含有非极性键 | B. | 1mol该分子中含8mol二氧化氮 | ||
| C. | 该物质既有氧化性又有还原性 | D. | 该物质爆炸产物是NO2、C02、H20 |
13.化学已渗透到人类生活的各个方面.下列说法正确的是( )
| A. | 为防止富脂食品氧化变质,常在包装袋中放入生石灰 | |
| B. | 铬是人体必需的微量元素,但铬过量会危害人体健康,其中六价铬的毒性最大.人体内六价铬超标,可以服用维生素C缓解毒性,说明维生素C具有氧化性 | |
| C. | 去年冬天的雾霾天气严重影响了人们的正常出行和生活节奏.为改善空气质量,可以加高工厂的烟囱,使烟尘和废气远离地表 | |
| D. | 硅酸钠是最简单的硅酸盐,是制备硅胶和木材防火剂的原料 |
10.硼烷是一种潜在的高能燃料,工业制取可用反应:B2O3+2Al+3H2=Al2O3+B2H6,下列有关说法正确的是( )
| A. | 该反应中氢气做还原剂,铝做氧化剂 | |
| B. | 在空气中Al2O3比 B2H6更稳定 | |
| C. | B2H6中存在极性键、非极性键、离子键 | |
| D. | 每生成1mol B2H6要消耗2molAlCl3 |
7.2008年北京奥运会火炬以中国传统祥云符号和纸卷轴为创意,由铝合金制成,使用的燃料为丙烷.下列说法不正确的是( )
| A. | 丙烷与甲烷互为同系物 | |
| B. | 通常条件下,丙烷性质稳定,不与酸、碱和氧化剂发生反应 | |
| C. | 丙烷燃烧是吸热反应 | |
| D. | 火炬燃料用丙烷比用煤油更环保 |
11.下列说法正确的是( )
| A. | 科学仪器的使用利于我们认识物质的微观世界,现在人们借助扫描隧道显微镜,应用SMT技术可以“看”到越来越细微的结构,并实现对原子或分子的操纵 | |
| B. | 利用外接直流电源保护铁质建筑物,属于电化学中牺牲阳极的阴极保护法 | |
| C. | 今年,来自德国、加拿大和我国复旦、清华大学的研究人员通过紧密合作,成功制备出了含+9铱元素的离子(IrOn+).在这种离子中,n=8 | |
| D. | 分类方法、统计方法、定量研究、实验方法和模型化方法等是化学研究的常用方法 |
12.与CH2=CH2→CH2Br-CH2Br的变化属于同一反应类型的是( )
| A. | CH3CHO→C2H5OH | B. | C2H5OH→CH2=CH2 | ||
| C. | 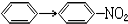 | D. | CH3COOH→CH3COOC2H5 |
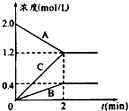 表示800℃时含有A、B、C三种气体的体系中各物质浓度(mol/L)随时间变化的情况如图所示
表示800℃时含有A、B、C三种气体的体系中各物质浓度(mol/L)随时间变化的情况如图所示 .
. .
.