题目内容
【题目】有一无色透明溶液,欲确定是否含有下列离子:![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() ,取该溶液的实验如下:
,取该溶液的实验如下:
实验步骤 | 实验现象 |
| 溶液变红色 |
| 有无色气体产生,气体遇空气可以变成红棕色 |
| 有白色沉淀生成 |
| 有稳定的白色沉淀生成,且不溶于稀硝酸 |
| 有白色沉淀生成,当NaOH过量时,沉淀部分溶解 |
由此判断,下列说法正确的是![]()
A.根据实验![]() 可以确定溶液中不含有
可以确定溶液中不含有![]() 和
和![]() ,因为这二个离子相对应的酸为弱酸
,因为这二个离子相对应的酸为弱酸
B.溶液中一定存在的离子是![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() ;溶液中肯定不存在的离子是:
;溶液中肯定不存在的离子是:![]() 、
、![]() 、
、![]() 、
、![]()
C.为进一步确定其它离子,应该补充焰色反应的实验来检验![]() 就可以
就可以
D.通过实验![]() 和
和![]() 就可以确定溶液中一定含有
就可以确定溶液中一定含有![]() ,一定不含有
,一定不含有![]() 、
、![]() 、
、![]() ,所以实验步骤
,所以实验步骤![]() 的设计是错误的
的设计是错误的
【答案】D
【解析】
因是一无色透明溶液,则不含有![]() ,由
,由![]() 取少量该溶液,加几滴甲基橙,溶液显红色,说明溶液显示酸性,所以
取少量该溶液,加几滴甲基橙,溶液显红色,说明溶液显示酸性,所以![]() 不存在;由
不存在;由![]() 取少量该溶液加热浓缩,加Cu片和浓硫酸,加热有无色气体产生,气体
取少量该溶液加热浓缩,加Cu片和浓硫酸,加热有无色气体产生,气体![]() 遇空气可以变成红棕色
遇空气可以变成红棕色![]() 二氧化氮
二氧化氮![]() ,说明溶液中含有
,说明溶液中含有![]() ,则一定不含有
,则一定不含有![]() ;由
;由![]() 取少量该溶液,加
取少量该溶液,加![]() 溶液,有白色沉淀生成,则含有
溶液,有白色沉淀生成,则含有![]() ;由
;由![]() 取
取![]() 中的上层清液,加
中的上层清液,加![]() 溶液,有稳定的白色沉淀生成,且不溶于稀硝酸,则含有
溶液,有稳定的白色沉淀生成,且不溶于稀硝酸,则含有![]() ,由于实验(3)所加的氯化钡溶液中含有
,由于实验(3)所加的氯化钡溶液中含有![]() ,所以原溶液中的
,所以原溶液中的![]() 是否存在不确定;由
是否存在不确定;由![]() 取少量该溶液,加入NaOH溶液有白色沉淀生成,当NaOH过量时,沉淀部分溶解,则含有铝离子、镁离子。则
取少量该溶液,加入NaOH溶液有白色沉淀生成,当NaOH过量时,沉淀部分溶解,则含有铝离子、镁离子。则
A、根据实验![]() 可以确定溶液中不含有
可以确定溶液中不含有![]() ,HI是强酸,不能确定I-是否存在,故A错误;
,HI是强酸,不能确定I-是否存在,故A错误;
B、溶液中一定存在的离子是![]() 、
、![]() 、
、![]() ,溶液中肯定不存在的离子是
,溶液中肯定不存在的离子是![]() 、
、![]() 、
、![]() 、
、![]() ,Cl-不能确定,故B错误;
,Cl-不能确定,故B错误;
C、钾离子、氯离子都是无法判断的离子,为进一步确定钾离子,应该补充焰色反应的实验来检验,但是氯离子的检验需要沉淀法,故C错误;
D、通过实验![]() 和
和![]() 就可以确定溶液中一定含有
就可以确定溶液中一定含有![]() ,和其反应的离子不存在,即一定不含有
,和其反应的离子不存在,即一定不含有![]() 、
、![]() 、
、![]() ,实验
,实验![]() 加了氯化钡溶液,含有氯离子,实验
加了氯化钡溶液,含有氯离子,实验![]() 再加硝酸银溶液检验氯离子是无效的,故D正确。
再加硝酸银溶液检验氯离子是无效的,故D正确。
故选D。

 全优测试卷系列答案
全优测试卷系列答案 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案【题目】氢气是一种清洁能源,又是合成氨工业的重要原料.已知氢气有多种制取方法:
①活泼金属![]() 如钠、钾
如钠、钾![]() 直接跟水反应;
直接跟水反应;
②金属![]() 如锌或铁或铝
如锌或铁或铝![]() 跟稀盐酸或稀硫酸反应;
跟稀盐酸或稀硫酸反应;
③电解水制氢气;
④由煤或焦炭跟水反应制取氢气:![]()
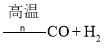 ;
;
⑤由天然气或重油制取氢气:![]()

![]() ;
;
(1)请你再补充一种制取氢气的方法,写出该反应的化学方程式 ______ .
(2)比较方法①和⑤: ______ g金属钠跟水反应与标准状况下![]()
![]() 跟水反应产生氢气的量相等.
跟水反应产生氢气的量相等.
(3)在甲、乙、丙3个容积均为2L的密闭容器中,于相同的温度下、使用相同的催化剂分别进行如下反应: 3H2(g)+N2(g) ![]() 2NH3(g),现按不同配比投入反应物,保持恒温、恒容,测得反应达到平衡时有关数据如下:
2NH3(g),现按不同配比投入反应物,保持恒温、恒容,测得反应达到平衡时有关数据如下:
容器 | 甲 | 乙 | 丙 |
反应物投入量 |
|
|
|
达到平衡的时间 |
| 5 | 8 |
| c |
| c |
|
|
|
|
混合气体密度 |
|
|
|
①分析表数据,下列关系正确的是 ______ ![]() 填写序号字母
填写序号字母![]() .
.
A.![]()
![]()
![]()
②在该温度下该反应的平衡常数![]() ______
______ ![]() 用含
用含![]() 的代数式表示
的代数式表示![]() .
.
(4)已知:![]() ;
;![]()
![]() ;
;![]()
则甲烷和![]() 反应生成
反应生成![]() 和
和![]() 的热化学方程式为 ______ .
的热化学方程式为 ______ .
(5)如图所示装置工作时均与![]() 有关.
有关.

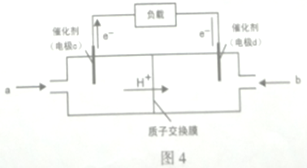
①图1所示装置中阳极的电极反应式为 ______ .
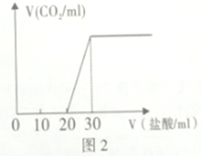
②图2所示装置中,通入![]() 的管口是 ______
的管口是 ______ ![]() 选填字母代号
选填字母代号![]() .
.
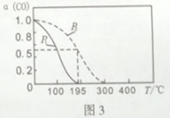
③某同学按图3所示装置进行实验,实验结束后,将玻璃管内固体物质冷却后,溶于稀硫酸,充分反应后,滴加KSCN溶液,溶液不变红,再滴入新制氯水,溶液变为红色.该同学据此得出结论:铁与水蒸气反应生成FeO和![]() 该结论 ______
该结论 ______ ![]() 填“严密”或“不严密”
填“严密”或“不严密”![]() ,你的理由是 ______
,你的理由是 ______ ![]() 用离子方程式表示
用离子方程式表示![]() .
.