题目内容
4.6种相邻短周期主族元素的相对位置如下表,M元素原子核外电子数是Y元素原子核外电子数的2倍,W元素原子的次外层电子数是最外层电子数的2倍.下列有关说法不正确的是( )| X | Y | Z | |
| W | M | Q |
| A. | W的最高价氧化物可以和Z的氢化物反应 | |
| B. | X、Y、Z三种元素的原子半径由大到小的顺序为Z>Y>X | |
| C. | X的含10个电子的气态氢化物可以与X的最高价氧化物对应的水化物溶液反应生成盐 | |
| D. | 工业上电解Q元素的钠盐溶液可获得一种含Q元素的消毒剂 |
分析 由相邻短周期主族元素的相对位置,可知X、Y、Z处于第二周期,W、M、Q处于第三周期,W元素原子的次外层电子数是最外层电子数的2倍,其最外层电子数为4,则W为Si,可推知X为N元素、Y为O元素、M为S元素、Z为F元素、Q为Cl,据此解答.
解答 解:由相邻短周期主族元素的相对位置,可知X、Y、Z处于第二周期,W、M、Q处于第三周期,W元素原子的次外层电子数是最外层电子数的2倍,其最外层电子数为4,则W为Si,可推知X为N元素、Y为O元素、M为S元素、Z为F元素、Q为Cl.
A.W的最高价氧化物为二氧化硅,Z的氢化物为HF,二氧化硅与HF反应生成四氟化硅与水,故A正确;
B.同周期自左而右原子半径减小,故原子半径X>Y>Z,故B错误;
C.X的含10个电子的气态氢化物为NH3,X的最高价氧化物对应的水化物为硝酸,二者反应生成硝酸铵,故C正确;
D.工业上电解NaCl溶液可获得NaClO消毒剂,故D正确,
故选B.
点评 本题考查结构性质位置关系应用,涉及元素周期律、元素化合物性质、电解池等,推断元素是解题关键,难度中等.

练习册系列答案
相关题目
6.下列说法正确的是 ( )
| A. | 紫色石蕊试液中通入二氧化硫,溶液先变红后褪色 | |
| B. | 将铜片放入浓硫酸中,无明显现象是因为铜片发生了钝化 | |
| C. | 硫粉在过量的纯氧中燃烧可以生成大量的SO3 | |
| D. | 富含硫黄的矿物在工业上可用于制造硫酸 |
7.用NA表示阿伏德罗常数,下列叙述正确的( )
| A. | 标准状况下,22.4LH2O含有的分子数为1 NA | |
| B. | 常温常压下,1.06g Na2CO3含有的Na+离子数为0.02 N | |
| C. | 通常状况下,1 NA个CO2分子占有的体积为22.4L | |
| D. | 标准状况下,22.4L CO2和SO2混合气中氧原子数为0.2NA |
12.设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 含4 mol HCl 的浓盐酸跟足量MnO2加热反应可制得 Cl2的分子数为NA | |
| B. | 将标准状况下 22.4LNO与11.2LO2混合后的体积约为 22.4L | |
| C. | 标准状况下,22.4L乙烯中含有σ键的数目为5NA | |
| D. | 1molC(金刚石)中含有C-C键的数目为4NA |
9.下列相关的离子方程式书写正确的是( )
| A. | NaHS溶液水解:HS-+H2O?S2-+H3O+ | |
| B. | 向Ca(C1O)2溶液中通入SO2:SO2+2ClO-+H2O=SO32-+2HClO | |
| C. | 硫酸与氢氧化钡溶液混合:H++SO42-+Ba2++OH-=BaSO4↓+H2O | |
| D. | 向NH4HSO4稀溶液中逐滴加入Ba(OH)2稀溶液至SO42ˉ刚好沉淀完全:Ba2++2OH-+NH4++H++SO42-=BaSO4↓+NH3•H2O+H2O |
16.在通常情况下能大量共存,并且可以用浓硫酸干燥的一组气体是( )
| A. | SO2、H2S、O2 | B. | CO、H2、Cl2 | C. | NO、H2、O2 | D. | HCl、CO、NH3 |
14.下列条件下的反应,放出H2最快的是( )
| 金属(粉末状)/mol | 酸的浓度和体积(mL) | 反应温度 | |||
| A | Mg | 0.1 | 3mol/L HCl | 10 | 20℃ |
| B | Al | 0.1 | 3mol/L HCl | 10 | 20℃ |
| C | Mg | 0.1 | 3mol/L CH3COOH | 10 | 20℃ |
| D | Mg | 0.1 | 3mol/L HNO3 | 10 | 30℃ |
| A. | A | B. | B | C. | C | D. | D |
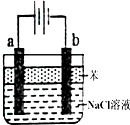 (1)用惰性电极电解饱和食盐水的反应方程式为:2NaCl+2H2O$\frac{\underline{\;电解\;}}{\;}$2NaOH+H2↑+Cl2↑.
(1)用惰性电极电解饱和食盐水的反应方程式为:2NaCl+2H2O$\frac{\underline{\;电解\;}}{\;}$2NaOH+H2↑+Cl2↑.
 (或写成
(或写成 R代表取代基或氢)
R代表取代基或氢) .
. .
.