题目内容
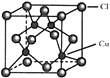
【题目】某学习小组用如图装置研究气体X的性质,气体X的主要成分是Cl2,其中含有少量水蒸气。请回答下列问题:

(1)分别描述B、C装置中的现象____;结合化学方程式及物质性质说明B、C装置中现象不同的原因____。
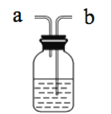
(2)Cl2是有毒气体,为了防止多余Cl2污染空气,可以在D处用如图装置进行尾气处理,用化学方程式表示该原理____。气体应该由____(填“a”或“b”)管通入。若要吸收224mLCl2(标况下),至少需要1mol/L的上述溶液____mL。
【答案】B中干燥的有色布条不褪色,C中湿润的有色布条褪色 Cl2没有漂白性,Cl2+H2O=HCl+HClO,HClO有漂白性 Cl2+2NaOH=NaCl+NaClO+H2O b 20
【解析】
本实验的目的是探究氯气具有漂白性的条件下,干燥氯气不具有漂白性,氯气和水反应生成盐酸和次氯酸,次氯酸具有漂白性,氯气有毒,应进行尾气处理,不能随意排放到空气中,一般用NaOH溶液吸收氯气。
(1)氯气与水反应生成氯化氢和次氯酸,氯化氢电离生成氢离子,次氯酸具有漂白性,B中干燥的有色布条不褪色,C中湿润的有色布条褪色。
结合化学方程式及物质性质说明B、C装置中现象不同的原因:Cl2没有漂白性,Cl2+H2O=HCl+HClO,HClO有漂白性 。
(2)氯气有毒,应进行尾气处理,不能随意排放到空气中,可用碱溶液来吸收,方程式为:Cl2+2NaOH=NaCl+NaClO+H2O。
在D处用如图装置进行尾气处理,实际上用的是洗气法,气体应该由b管通入;
若要吸收224mLCl2(标况下),至少需要1mol/L的上述溶液:
Cl2+2NaOH=NaCl+NaClO+H2O
22.4L 2mol
224mL 1mol/L×VmL
![]() =
=![]()
解得V=20。

 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案【题目】已知25℃时部分弱电解质的电离平衡常数数据如表所示,回答下列问题:
化学式 | CH3COOH | H2CO3 | HClO |
电离平衡常数 | Ka=1.8×10﹣5 | Ka1=4.3×10﹣7 Ka2=5.6×10﹣11 | Ka=3.0×10﹣8 |
(1)物质的量浓度均为0.1molL﹣1的四种溶液:pH由小到大排列的顺序是_______(用编号填写)
a.CH3COONa b.Na2CO3 c.NaClO d.NaHCO3
(2)常温下,0.1molL﹣1 CH3COOH溶液加水稀释过程中,下列表达式的数据变大的是_____(填字母)_______
A. c(H+) B.![]() C. c(H+)c(OH﹣) D.
C. c(H+)c(OH﹣) D. ![]() E.
E. ![]()
(3)写出向次氯酸钠溶液中通入少量二氧化碳的离子方程式:__________________
(4)25℃时,CH3COOH与CH3COONa的混合溶液,若测得混合液pH=6,则溶液中
c(CH3COO﹣)﹣c(Na+)=________(填准确数值)。
(5)25℃时,将a molL﹣1的醋酸与b molL﹣1氢氧化钠等体积混合,反应后溶液恰好显中性,用a、b表示醋酸的电离平衡常数为____________________________________
(6)标准状况下,将1.12L CO2通入100mL 1molL﹣1的NaOH溶液中,用溶液中微粒的浓度符号完成下列等式: c(OH﹣)=2c(H2CO3)+_________________________