题目内容
【题目】关于![]() 溶液,下列判断不正确的是 ( )
溶液,下列判断不正确的是 ( )
A. 粒子种类与![]() 溶液相同
溶液相同
B. 升高温度,![]() 增大
增大
C. 加入![]() 溶液,
溶液,![]() 减小
减小
D. ![]()
【答案】B
【解析】
从溶质的溶解直至水的电离,可知溶液中粒子种类;根据外因对化学平衡的影响分析浓度变化;由溶液的电中性原理可写电荷守恒关系。
A项:溶液中Na2CO3完全电离Na2CO3=2Na++CO32-,CO32-分两步水解CO32-+H2O![]() HCO3-+OH-,HCO3-+H2O
HCO3-+OH-,HCO3-+H2O![]() H2CO3+OH- ,水的电离H2O
H2CO3+OH- ,水的电离H2O![]() H++OH- 。同理可写出
H++OH- 。同理可写出![]() 溶液的各种过程,两溶液中粒子种类相同,A项正确;
溶液的各种过程,两溶液中粒子种类相同,A项正确;
B项:CO32-水解过程吸热,升高温度使水解平衡右移,![]() 减小,B项错误;
减小,B项错误;
C项:加入![]() 溶液,Ca2+与CO32-结合生成难溶于水的CaCO3沉淀,使
溶液,Ca2+与CO32-结合生成难溶于水的CaCO3沉淀,使![]() 减小,C项正确;
减小,C项正确;
D项:水溶液都是电中性的,符合电荷守恒![]() ,D项正确。
,D项正确。
本题选B。

 精英口算卡系列答案
精英口算卡系列答案 应用题点拨系列答案
应用题点拨系列答案【题目】铁及其化合物有重要且广泛的应用
(1)基态Fe2+的价层电子排布图为_____________
(2)检验Fe3+可以用KSCN溶液,写出SCN-的一种等电子体分子_______。
(3)部分电离能数据如下表:
元素 | Mn | Fe | |
电离能 |
| 717 | 759 |
| 1 509 | 1 561 | |
| 3 248 | 2 957 | |
根据表中数据可知,气态![]() 再失去一个电子比气态
再失去一个电子比气态![]() 再失去一个电子难,其原因是___________________________。
再失去一个电子难,其原因是___________________________。
(4)过渡金属原子可以与CO分子形成配合物,配合物价电子总数符合“18电子规则”。如Cr可以与CO形成![]() 分子:价电子总数
分子:价电子总数![]() 的价电子数
的价电子数![]() 提供电子数
提供电子数![]() .Fe原子也能与CO形成配合物,其化学式为________.
.Fe原子也能与CO形成配合物,其化学式为________.
(5)已知Fe单质有如图所示的两种常见堆积方式:
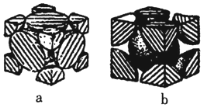

其中属于体心立方密堆积的是______![]() 填“a”或“b”
填“a”或“b”![]() ;若单质Fe按a方式紧密堆积,设原子半径为rpm,图中晶胞的棱长为_________
;若单质Fe按a方式紧密堆积,设原子半径为rpm,图中晶胞的棱长为_________
(6)FeS2晶体的晶胞如图(c)所示。晶胞边长为a nm、FeS2相对式量为M,阿伏加德罗常数的值为NA,其晶体密度的计算表达式为___________g·cm3。