题目内容
| A.变蓝色 | B.变深 |
| C.变浅 | D.不变 |
C
在0.1 mol·L-1氨水中存在平衡NH3·H2O NH
NH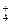 +OH-,碱性溶液遇酚酞呈现红色。若向其中加入少量的NH4Cl晶体,由于溶液中c(NH
+OH-,碱性溶液遇酚酞呈现红色。若向其中加入少量的NH4Cl晶体,由于溶液中c(NH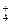 )的增大,导致上述平衡往逆反应方向移动。则溶液的颜色变浅。
)的增大,导致上述平衡往逆反应方向移动。则溶液的颜色变浅。
 NH
NH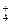 +OH-,碱性溶液遇酚酞呈现红色。若向其中加入少量的NH4Cl晶体,由于溶液中c(NH
+OH-,碱性溶液遇酚酞呈现红色。若向其中加入少量的NH4Cl晶体,由于溶液中c(NH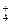 )的增大,导致上述平衡往逆反应方向移动。则溶液的颜色变浅。
)的增大,导致上述平衡往逆反应方向移动。则溶液的颜色变浅。
练习册系列答案
相关题目
题目内容
| A.变蓝色 | B.变深 |
| C.变浅 | D.不变 |
 NH
NH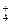 +OH-,碱性溶液遇酚酞呈现红色。若向其中加入少量的NH4Cl晶体,由于溶液中c(NH
+OH-,碱性溶液遇酚酞呈现红色。若向其中加入少量的NH4Cl晶体,由于溶液中c(NH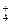 )的增大,导致上述平衡往逆反应方向移动。则溶液的颜色变浅。
)的增大,导致上述平衡往逆反应方向移动。则溶液的颜色变浅。