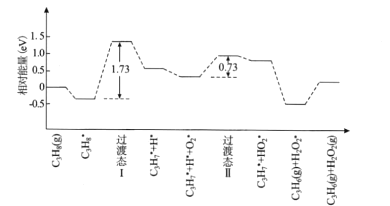
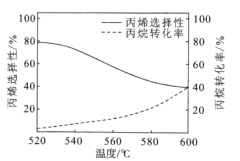
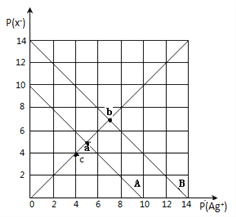
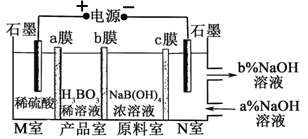
题目内容
【题目】某学生做同主族元素性质递变规律的实验时,自己设计了一套实验方案,并记录了有关实验现象.现在请你帮助该学生整理并完成实验报告.
(1)实验目的: ______
(2)实验用品:药品:氯水、溴水、溴化钠溶液、碘化钾溶液、四氯化碳.
仪器:① ______ ;② ______ ![]() 请填写两件主要的玻璃仪器
请填写两件主要的玻璃仪器![]()
(3)实验内容:
序号 | 实验方案 | 实验现象 |
① | 将少量氯水滴入盛有少量NaBr溶液的试管中,振荡;再滴入少量四氯化碳,振荡 | 加入氯水后,溶液由无色变为橙色,滴入四氯化碳后,水层颜色变浅,四氯化碳层 |
② | 将少量溴水滴入盛有少量KI溶液的试管中,振荡;再滴入少量四氯化碳,振荡 | 加入溴水后,溶液由无色变为黄色,滴入四氯化碳后,水层颜色变浅,四氯化碳层 |
(4)实验结论: ______ .
(5)问题和讨论:请用结构理论简单说明得出上述结论的原因. ______ .
【答案】探究同一主族元素性质的递变规律 试管 胶头滴管 同一主族元素,自上而下,元素的非金属性依次减弱 同一主族元素,自上而下,元素原子的电子层数增多,原子半径增大,原子核对最外层电子的吸引力逐渐减弱
【解析】
氯气具有氧化性,能将溴离子氧化为溴单质,溴单质在有机层显示橙红色;溴单质能将碘离子氧化为碘单质,碘单质在有机层中显示紫红色,结合原子结构与元素性质的关系分析解答。
(1)根据实验现象结合氧化剂的氧化性强于氧化产物的氧化性来得出同主族元素性质的递变规律,故答案为:探究同一主族元素性质的递变规律;
(2)根据实验步骤,实验在试管内进行,再滴入少量四氯化碳,振荡,滴加液体用胶头滴管,故答案为:试管;胶头滴管;
(4)氯气能将溴离子从其水溶液中置换出来,而溴单质能将碘离子从其水溶液中置换出来,说明氧化性是氯气强于溴单质,溴单质强于碘单质,元素的非金属性越强,即非金属性:Cl>Br>I,得出同主族元素性质的递变规律:同主族元素性质相似,且从上到下,元素的非金属性逐渐减弱,故答案为:同一主族元素,自上而下,元素的非金属性依次减弱;
(5)依据原子理论解释为:同一主族元素,自上而下,随原子序数的增加,原子半径逐渐增大,原子核对于核外电子的引力渐强,原子失电子能力减弱,故答案为:同一主族元素,自上而下,元素原子的电子层数增多,原子半径增大,原子核对最外层电子的吸引力逐渐减弱。