题目内容
【题目】实验室可用环己醇制备环己酮,使用的氧化剂可以是次氯酸钠、重铬酸钾等。

已知:环己醇沸点:160.8℃,微溶于水;
环己酮沸点:155.6℃,微溶于水;
醋酸沸点117.9℃,和水以任意比例互溶。
下列装置分别是产品的合成装置和精制装置示意图:

合成实验过程如下:
向装有搅拌器、滴液漏斗和温度计的三颈烧瓶中依次加入5.2mL环己醇和25mL冰醋酸。开动搅拌器,将40mL次氯酸钠溶液逐渐加入到反应瓶中,并使瓶内温度维持在30~35℃,用磁性搅拌器搅拌5min。然后,在室温下继续搅拌30min后,在合成装置中再加入30mL水、3g氯化铝和几粒沸石,加热蒸馏至馏出液无油珠滴出为止。回答下列问题:
(1)在合成装置中,甲装置的名称是_____________。
(2)三颈烧瓶的容量为_____________(填“50mL"、“100mL”或“250mL")。
(3)滴液漏斗具有特殊的结构,主要目的是_____________。
(4)蒸馏完成后,向馏出液中分批加入无水碳酸钠至反应液呈中性为止,其目的是_____________。然后加入精制食盐使之变成饱和溶液,将混合液倒入_____________中,分离得到有机层。
(5)用如图对粗产品进行精制,蒸馏收集_____________℃的馏分。
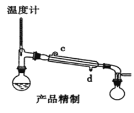
(6)检验环己酮是否纯净,可使用的试剂为_____________。
A.重铬酸钾溶液B.金属钠C.新制的氢氧化铜悬浊液D.醋酸溶液
【答案】直形冷凝管 250mL 平衡压强,使所加液体能顺利滴入三颈烧瓶中 除去产品中混有的醋酸杂质 分液漏斗 155.6 AB
【解析】
根据整个反应过程中所加液体的总体积大于100mL可知,反应需选250 mL的三颈烧瓶;为了使所加液体能顺利滴入三颈瓶中采用滴液漏斗;在装有搅拌器、滴液漏斗和温度计的三颈烧瓶中,由环己醇和冰醋酸、次氯酸钠等物质加热反应后蒸馏得到环己酮的粗产品;因环己酮沸点为155.6℃,故可收集155.6℃时的馏出液,但由于醋酸沸点为117.9℃,所以馏出液中含有杂质醋酸,为了纯化产物,因醋酸能和水以任意比例互溶,且与碳酸钠反应后的产物不溶于有机物溶液中,故向馏出液中分批加入无水碳酸钠至反应液呈中性为止以除去产品中混有的醋酸杂质。由于有机物在盐溶液中的溶解度小,盐溶液能减少有机物的溶解损失,所以加入精制食盐使之变成饱和溶液,将混合液倒入分液漏斗中,分离即可得到有机层。
(1)在合成装置中,甲起冷凝作用,甲装置的名称是直形冷凝管;
(2) 三颈烧瓶中依次加入5.2mL环己醇和25mL冰醋酸,将40mL次氯酸钠溶液逐渐加入到反应瓶,在合成装置中再加入30mL水、3g氯化铝和几粒沸石,可知溶液的总体积大于100mL,所以选250 mL的三颈烧瓶;
(3)滴液漏斗具有特殊的结构,使三颈瓶内的压强与漏斗内的压强相等,使所加液体能顺利滴入三颈瓶中;
(4)Na2CO3+2CH3COOH=2CH3COONa+H2O+CO2↑,馏出液中分批加入无水碳酸钠至反应液呈中性为止,其目的是将反应混合物中醋酸变成醋酸钠,便于分离;产品在精制饱和食盐溶液中溶解度小,有利于分层,用分液漏斗可将其分离出来;
(5)环己酮的沸点:155.6℃,所以收集155.6℃的馏分;
(6)A.环己醇能被重铬酸钾溶液氧化,重铬酸钾溶液变成绿色,若两者混合不显示绿色,则说明产品中不含杂质环己醇,A符合题意;
B.环己醇中的醇羟基能与钠发生置换反应,生成H2,若两者混合不产生氢气则说明产品中不含杂质环己醇,B符合题意;
C.新制的氢氧化铜悬浊液与两者均不反应,无法检验环己酮是否纯净,C不符合题意;
D.醋酸本来就是产物中所含的杂质,不能用其来检验环己酮是否纯净,D不符合题意;
答案选AB。

【题目】氢氧化亚铁易被氧化,制取过程要隔绝空气。现用铁屑、稀硫酸、氢氧化钠溶液制备氢氧化亚铁并观察其颜色,改进装置如下:

(1)稀硫酸应放在___(填写仪器名称)中。
(2)本实验通过关闭开关___、打开开关___,将仪器中的空气排尽后,后续实验就可观察到氢氧化亚铁的颜色。
(3)在FeSO4溶液中加入(NH4)2SO4固体可制备莫尔盐晶体[(NH4)2SO4·FeSO4·6H2O](相对分子质量392),该晶体比一般亚铁盐稳定,不易被氧化,易溶于水,不溶于乙醇。
①为洗涤(NH4)2SO4·FeSO4·6H2O粗产品,下列方法中最合适的是___。
a.用冷水洗 b.先用冷水洗,后用无水乙醇洗
c.用30%的乙醇溶液洗 d.用90%的乙醇溶液洗
②为了测定产品的纯度,称取ag产品溶于水,配制成500mL溶液。每次取待测液20.00mL,用浓度为bmol/L的酸性KMnO4溶液滴定,实验结果记录如下:
实验次数 | 第一次 | 第二次 | 第三次 |
消耗酸性高锰酸钾溶液体积/mL | 20.02 | 19.98 | 20.52 |
滴定过程中发生反应的离子方程式为___。滴定终点的现象是___。
通过实验数据计算的该产品纯度为___(用字母a、b表示)。