题目内容
19.下列有关分类的观点正确的是( )①氨水、醋酸、氢氧化铝都属于弱电解质
②生物质能、沼气和乙醉都是可再生能源
③碳素钢、不锈钢和目前流通的硬币都属于合金
④铅蓄电池、锂电池、碱性锌锰电池都属于二次电池
⑤由苯制取溴苯、硝基苯、环己烷的反应都属于取代反应.
| A. | ①② | B. | ②③ | C. | ③④ | D. | ③⑤ |
分析 ①氨水为混合物,既不是电解质也不是非电解质;
②生物质能、沼气和乙醇都可再生;
③碳素钢、不锈钢为铁的合金,硬币为铝的合金、铜的合金;
④碱性锌锰电池为一次电池;
⑤苯制备环己烷发生加成反应;
解答 ①氨水为混合物,既不是电解质也不是非电解质,而醋酸、氢氧化铝都属于弱电解质,故①错误;
②生物质能、沼气和乙醇都可再生,所以均属于可再生资源,故②正确;
③碳素钢、不锈钢为铁的合金,硬币为铝的合金、铜的合金,则碳素钢、不锈钢和目前流通的硬币都属于合金,故③正确;
④碱性锌锰电池为一次电池,而铅蓄电池、锂电池都属于二次电池,可重复使用,故④错误;
⑤苯制备环己烷发生加成反应,而由苯制取溴苯、硝基苯的反应都属于取代反应,故⑤错误;
故选B.
点评 本题考查较综合,涉及有机反应、原电池、合金、电解质的判断、资源及分类等,综合性较强,注重基础知识的考查,有利于学生双基的巩固,题目难度不大.

练习册系列答案
相关题目
9.某小分子抗癌药物的分子结构如图所示,下列说法正确的是( )
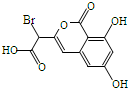

| A. | 1mol该有机物最多可以和5mol NaOH反应 | |
| B. | 该有机物容易发生加成、取代、中和、消去等反应 | |
| C. | 该有机物遇FeCl3溶液不变色,但可使酸性KMnO4溶液褪色 | |
| D. | 1mol该有机物与浓溴水或氢气反应,最多消耗3mol Br2或6molH2 |
10.短周期主族金属元素甲、乙、丙在元素周期表中的相对位置如表所示,下列判断不正确的是( )
| 甲 | |
| 乙 | 丙 |
| A. | 原子半径:甲<乙 | |
| B. | 最外层电子数:甲>乙 | |
| C. | 最高价氧化物对应的水化物的碱性:丙>乙 | |
| D. | 金属性:丙<乙 |
7.已知X、Y和Z三种元素的原子序数之和等于42.X元素原子的4p轨道上有3个未成对电子,Y元素原子的2p轨道上有2个未成对电子,X跟Y可形成化合物X2Y3,Z元素可形成正一价离子.下列说法正确的是( )
| A. | Y元素的基态原子核外原子排布式为1s22s22p2 | |
| B. | Y元素与Z元素可以形成化合物Z2Y2 | |
| C. | X元素的基态原子中3个未成对电子的能量不相同 | |
| D. | X元素与Z元素可以形成离子化合物XZ3 |
14.对于反应CaH2+2H2O═Ca(OH)2+2H2↑,有下列判断:①H2只是氧化产物;②H2只是还原产物;③H2O是氧化剂;④CaH2中的氢元素被还原;⑤此反应中氧化产物与还原产物的原子个数之比是1:1,
上述判断中正确的是( )
上述判断中正确的是( )
| A. | ①②③ | B. | ③⑤ | C. | ②④ | D. | ④⑤ |
11.下列说法正确的是( )
| A. | SiH4比PH3稳定 | |
| B. | 短周期元素形成离子后,最外层电子都达到8电子稳定结构 | |
| C. | Na和Cs属于第ⅠA族元素,Cs失电子能力比Na的强 | |
| D. | 某元素原子最外层只有一个电子,它跟卤素结合时所形成的化学键一定是离子键 |
8.下列物质中不能与金属钠反应的是( )
| A. | 苯 | B. | 水 | C. | 氧气 | D. | 乙醇 |
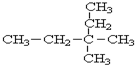 3,3-二甲基戊烷.
3,3-二甲基戊烷. .再将反应后的混合物转移到分液漏斗中,振荡、静置,然后分液.从分液漏斗放出下层液体,加入适量盐酸,再将其分成两份:向一份溶液中加入三氯化铁溶液,出现的现象是溶液呈紫色;向另一份溶液中加入浓溴水,反应的化学方程式为
.再将反应后的混合物转移到分液漏斗中,振荡、静置,然后分液.从分液漏斗放出下层液体,加入适量盐酸,再将其分成两份:向一份溶液中加入三氯化铁溶液,出现的现象是溶液呈紫色;向另一份溶液中加入浓溴水,反应的化学方程式为 .从分液漏斗上口倒出的液体是苯.
.从分液漏斗上口倒出的液体是苯.