题目内容
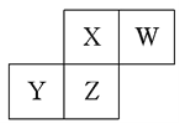
【题目】已知热化学方程式C2H2(g)+![]() O2(g)=2CO2(g)+H2O(g) △H=-1256kJ/mol,下列说法正确的是( )
O2(g)=2CO2(g)+H2O(g) △H=-1256kJ/mol,下列说法正确的是( )
A.乙炔的燃烧热为1256kJ·mol-1
B.若生成2mol液态水,则放出的热量为2512 kJ·mol-1
C.若转移10mol电子,则消耗2.5mo1 O2
D.若形成4mol碳氧共用电子对,则放出的热量为2512kJ
【答案】C
【解析】
A.燃烧热是指在一定条件下,1mol物质完全燃烧生成稳定的氧化物时所放出的热量,水的稳定状态是液态,故A错误;
B.生成2mol气态水时,放出2512 kJ·mol-1热量,故B错误;
C.1mol氧气得到4mol电子,所以转移10mol电子,需要![]() =2.5mol氧气,故C正确;
=2.5mol氧气,故C正确;
D.形成4mol碳氧共用电子对说明反应生成2molCO2,放出的热量为1256kJ,故D错误;
故选C。

【题目】一定量的铁粉在氯气中充分燃烧后,将所得固体完全溶于稀盐酸,制得溶液A。
(1)铁在氯气中燃烧的化学方程式是____________________________。
(2)推测A中可能含有的金属阳离子:①Fe3+;②只有Fe2+;③______。
甲同学为探究溶液的组成,实验如下:
实验步骤 | 实验现象 | 实验结论及反应离子方程式 |
取少量溶液A于试管中,加入KSCN溶液。 | ________ | 假设②不成立,假设①或③成立;反应的离子方程式是_____________ 。 |
(3)乙同学继续探究溶液A的组成。
查阅资料:16HCl+2KMnO4=2KCl+2MnCl2+5Cl2↑+8H2O
实验过程:另取少量溶液A于试管中,逐滴加入酸性KMnO4溶液,充分振荡,KMnO4紫色褪去。
实验结论:__________(填写字母序号)。
a.可能有Fe2+ b.可能无Fe2+ c.一定有Fe2+
(4)结论:A中含有的阳离子是_________,简述理由:________________。