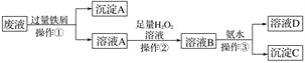
题目内容
【题目】下列事实不能用勒夏特列原理解释的是( )
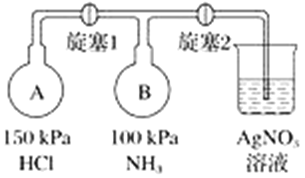
A. 溴水中有下列平衡Br2+H2O![]() HBr+HBrO,当加入硝酸银溶液后,溶液颜色变浅
HBr+HBrO,当加入硝酸银溶液后,溶液颜色变浅
B. 已知, N2 (g) + 3 H2(g)![]() 2NH3(g) △H﹤0 ,为提高氨的产率,理论上应采取降低温度的措施
2NH3(g) △H﹤0 ,为提高氨的产率,理论上应采取降低温度的措施
C. 反应CO(g)+NO2(g)![]() CO2(g)+NO(g)△H﹤0,达平衡后,升高温度体系颜色变深
CO2(g)+NO(g)△H﹤0,达平衡后,升高温度体系颜色变深
D. 对于2HI(g)![]() H2(g)+I2(g),达平衡后,缩小容器体积可使体系颜色变深
H2(g)+I2(g),达平衡后,缩小容器体积可使体系颜色变深
【答案】D
【解析】A、加入硝酸银溶液后,银离子消耗溴水中的溴离子,生成溴化银沉淀,溶液中溴离子浓度减小,平衡向着正向移动,能够用勒夏特列原理解释,选项A错误;B、由于合成氨反应是放热反应,降低温度,平衡向着放热方向移动,即向着正向移动,能够用勒夏特列原理解释,选项B错误;C、反应CO(g)+NO2(g)![]() CO2(g)+NO(g)△H﹤0,达平衡后,升高温度平衡向逆反应方向移动,体系颜色变深,能够用勒夏特列原理解释,选项C错误;D、通入氢气后氢气浓度增大,平衡向着氢气浓度减小的方向移动,不能够用勒夏特列原理解释,选项D正确。答案选D。
CO2(g)+NO(g)△H﹤0,达平衡后,升高温度平衡向逆反应方向移动,体系颜色变深,能够用勒夏特列原理解释,选项C错误;D、通入氢气后氢气浓度增大,平衡向着氢气浓度减小的方向移动,不能够用勒夏特列原理解释,选项D正确。答案选D。

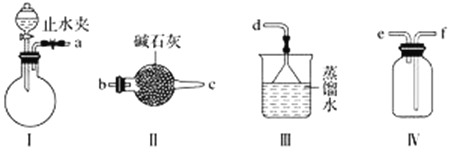
【题目】利用如图所示装置进行下列实验,能得出相应实验结论的是( )

选项 | ① | ② | ③ | 实验结论 |
A | 稀盐酸 | CaCO3 | Na2SiO3溶液 | 非金属性:Cl>C>Si |
B | 浓硫酸 | 蔗糖 | Ba(NO3)2溶液 | 验证SO2与可溶性钡盐可生成白色沉淀 |
C | 浓氨水 | 生石灰 | 酚酞溶液 | 氨气的水溶液呈碱性 |
D | 浓硝酸 | Fe | NaOH溶液 | 铁和浓硝酸反应可生成NO2 |
A. A B. B C. C D. D
【题目】已知:①H2(g)+![]() O2(g)=H2O(g) ΔH1=-241.8kJ·mol-1;
O2(g)=H2O(g) ΔH1=-241.8kJ·mol-1;
②H2(g)+![]() O2(g)=H2O(l) ΔH2=-285.8kJ·mol-1。
O2(g)=H2O(l) ΔH2=-285.8kJ·mol-1。
气态分子中的化学键 | 断开1mol化学键所需的能量/kJ |
O—H | 465 |
O=O | 498 |
下列说法不正确的是( )
A.氢气的燃烧热ΔH=-241.8kJ·mol-1
B.断开1molH—H键需要吸收439.2kJ的能量
C.相同条件下,1molH2O(g)比1molH2O(l)能量高
D.18gH2O(l)完全分解生成氢气和氧气,需要吸收285.8kJ的能量