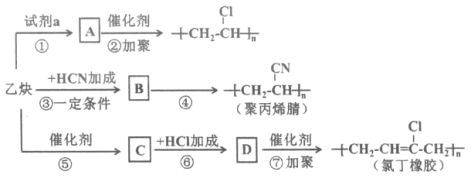
题目内容
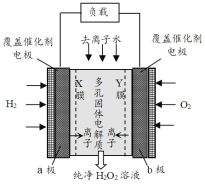
【题目】2019年 11月《Science》杂志报道了王浩天教授团队发明的制取 H2O2 的绿色方法,原理如图所示(已知:H2O2![]() H++HO2-,Ka=2.4×10-12。下列说错误的是( )
H++HO2-,Ka=2.4×10-12。下列说错误的是( )
A.X膜为阳离子交换膜
B.每生成 1mol H2O2外电路通过4mol e-
C.催化剂可加快单位时间内反应中电子的转移数目
D.b极上的电极反应为:O2+ H2O + 2e- = HO2 + OH-
【答案】B
【解析】
通入H2的电极为原电池的负极,发生氧化反应,其电极反应式为:H2-2e-= 2H+,通入O2的电极为原电池的正极,发生还原反应,其电极反应式为:O2+H2O+2e-=HO2-+OH-。
A. 在H2、O2燃料电池中,通入H2的电极为原电池负极,氢气失电子生成H+,因此X膜为选择性阳离子交换膜,A正确;
B. 原电池正极上O2得电子生成HO2-,氧元素的化合价由0价降低为-1价,因此每生成1molH2O2电极上流过2mole-,B错误;
C. 催化剂能降低活化能,加快反应速率,促进反应中电子的转移,C正确;
D. b极上通入氧气,为原电池正极,O2得电子生成HO2-,电极反应式为:O2+H2O+2e-= HO2-+OH-,D正确;故答案为:B。

 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案【题目】恒温恒容下,向2L密闭容器中加入MgSO4(s)和CO(g),发生反应:MgSO4(s)+CO(g)MgO(s)+CO2(g)+SO2(g)反应过程中测定的部分数据见下表:
反应时间/min | n(MgSO4)/mol | n(CO)/mol | n(CO2)/mol |
0 | 2.00 | 2.00 | 0 |
2 | 0.80 | ||
4 | 1.20 |
下列说法正确的是( )
A.反应在0~2min内的平均速率为v(SO2)=0.6molL-1min-1
B.反应在2~4min内容器内气体的密度没有变化
C.若升高温度,反应的平衡常数变为1.00,则正反应为放热反应
D.保持其他条件不变,起始时向容器中充入1.00molMgSO4和1.00molCO,到达平衡时n(CO2)<0.60mol
【题目】某矿渣的成分为Cu2O、Al2O3、Fe2O3、SiO2,工业上用该矿渣获取铜和胆矾的操作流程如图:

已知:①Cu2O+2H+=Cu+Cu2++H2O。
②部分阳离子以氢氧化物形式沉淀时溶液的pH如下表所示:
沉淀物 | Cu(OH)2 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 |
开始沉淀pH | 5.4 | 4.0 | 2.7 | 5.8 |
沉淀完全pH | 6.7 | 5.2 | 3.7 | 8.8 |
(1)为了加快反应Ⅰ的速率,可以采取的措施是__(任写1条)。
(2)固体混合物A中的成分是__。
(3)反应Ⅰ完成后,铁元素的存在形式为__(填离子符号);检验该离子常用的方法之一是:取少量含该离子的溶液于试管中,滴加几滴含有+3价铁元素的配合物溶液,会产生沉淀.写出该反应的离子方程式__。
(4)操作1主要包括:__、__、__。洗涤CuSO4·5H2O粗产品不能用大量水洗,而用冰水洗涤。原因是__。
(5)用NaClO调pH可以生成沉淀B,利用题中所给信息分析沉淀B为___,该反应中氧化剂与还原剂的物质的量之比为___。
(6)用NaOH调pH可以生成沉淀C,利用题中所给信息分析y的范围为___。