题目内容
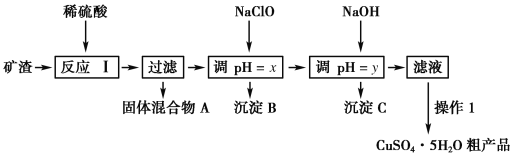
【题目】某矿渣的成分为Cu2O、Al2O3、Fe2O3、SiO2,工业上用该矿渣获取铜和胆矾的操作流程如图:
已知:①Cu2O+2H+=Cu+Cu2++H2O。
②部分阳离子以氢氧化物形式沉淀时溶液的pH如下表所示:
沉淀物 | Cu(OH)2 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 |
开始沉淀pH | 5.4 | 4.0 | 2.7 | 5.8 |
沉淀完全pH | 6.7 | 5.2 | 3.7 | 8.8 |
(1)为了加快反应Ⅰ的速率,可以采取的措施是__(任写1条)。
(2)固体混合物A中的成分是__。
(3)反应Ⅰ完成后,铁元素的存在形式为__(填离子符号);检验该离子常用的方法之一是:取少量含该离子的溶液于试管中,滴加几滴含有+3价铁元素的配合物溶液,会产生沉淀.写出该反应的离子方程式__。
(4)操作1主要包括:__、__、__。洗涤CuSO4·5H2O粗产品不能用大量水洗,而用冰水洗涤。原因是__。
(5)用NaClO调pH可以生成沉淀B,利用题中所给信息分析沉淀B为___,该反应中氧化剂与还原剂的物质的量之比为___。
(6)用NaOH调pH可以生成沉淀C,利用题中所给信息分析y的范围为___。
【答案】适当升高温度;不断搅拌;将矿渣粉碎;适当增大硫酸的浓度等 SiO2、Cu Fe2+ 3Fe2++2[Fe(CN)6]3-=Fe3[Fe(CN)6]2↓ 蒸发浓缩 冷却结晶 过滤 冰水既可以洗去晶体表面的杂质离子,又可以减少晶体的损失 Fe(OH)3 1:2 5.2-5.4或5.2≤pH<5.4
【解析】
根据已知,分析工艺流程图,矿渣的成分为Cu2O、Al2O3、Fe2O3、SiO2,在加入稀硫酸溶解经过滤后得到CuSO4、Al2(SO4)3、FeSO4溶液和固体混合物A(主要成分为Cu单质和SiO2),再加入NaClO氧化Fe2+并调节pH至3.7≤pH<4.0,将Fe3+沉淀,再加入NaOH调节pH至5.2≤pH<5.4,将Al3+沉淀,滤液再经过蒸发浓缩、冷却结晶、过滤得到CuSO4·5H2O粗产品,据此分析解答问题。
(1)由于矿渣为固体,所以为了加快反应的速率,可以采取的措施是将固体粉碎,也可以适当升高反应的温度,或增大反应物H2SO4浓度等措施,故答案为:适当升高温度;不断搅拌;将矿渣粉碎;适当增大硫酸的浓度等;
(2)SiO2是酸性氧化物,不能与酸发生反应,其它金属氧化物Cu2O、Al2O3、Fe2O3与硫酸发生反应Cu、CuSO4、Al2(SO4)3、FeSO4,因此发生反Ⅰ后过滤出的固体混合物A中的成分是SiO2和Cu,故答案为:SiO2、Cu;
(3)因为在反应Ⅰ中Fe2O3与硫酸发生反应生成Fe2(SO4)3,而Cu2O与稀硫酸生成的Cu又与Fe2(SO4)3发生氧化还原生成Cu2+和Fe2+,则铁元素的存在形式为Fe2+,检验Fe2+用铁氰化钾溶液,发生的反应方程式为3Fe2++2[Fe(CN)6]3-=Fe3[Fe(CN)6]2↓,故答案为:Fe2+;3Fe2++2[Fe(CN)6]3-=Fe3[Fe(CN)6]2↓;
(4)从硫酸铜溶液中制取硫酸铜晶体的操作主要包括:蒸发浓缩、冷却结晶、过滤,由于CuSO4溶解于水,且温度越高,溶解度越大,若用冰水既可以洗去晶体表面的杂质离子,又可以减少晶体的损失,故答案为:蒸发浓缩;冷却结晶;过滤;冰水既可以洗去晶体表面的杂质离子,又可以减少晶体的损失;
(5)NaClO具有氧化性,Fe2+具有还原性,用NaClO调节pH时,反应生成Fe(OH)3沉淀和具有漂白作用的HClO,反应的离子方程式为:7ClO-+2Fe2++2H++5H2O===2Fe(OH)3↓+Cl-+6HClO,其中氧化剂和还原剂的比值为1:2,故答案为:Fe(OH)3;1:2;
(6)结合表格数据,Al3+完全沉淀时的pH为5.2,而Cu2+开始沉淀的pH为5.4,故加入NaOH调节pH至5.2≤pH<5.4,将Al3+沉淀,而Cu2+不沉淀,故答案为:5.2-5.4或5.2≤pH<5.4。

 孟建平错题本系列答案
孟建平错题本系列答案 超能学典应用题题卡系列答案
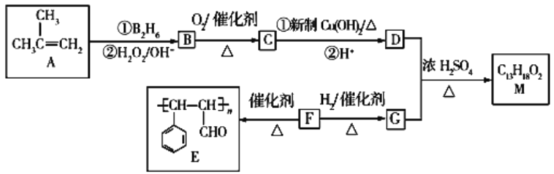
超能学典应用题题卡系列答案【题目】肉桂酸是合成香料、化妆品、医药、浆料和感光树脂等的重要原料,其结构简式是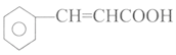 。
。
I.写出肉桂酸的反式结构: __________。
II.实验室可用下列反应制取肉桂酸。
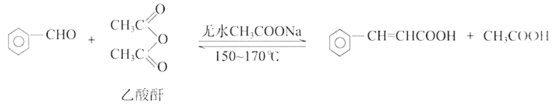
已知药品的相关数据如下:
苯甲醛 | 乙酸酐 | 肉桂酸 | 乙酸 | |
溶解度(25℃,g/100g 水) | 0.3 | 遇水水解 | 0.04 | 互溶 |
相对分子质量 | 106 | 102 | 148 | 60 |
实验步骤如下:
第一步合成:向烧瓶中依次加入研细的无水醋酸钠、5.3g 苯甲醛和6.0g乙酸酐,振荡使之混合均匀。在150~ 170℃加热1小时,保持微沸状态。第二步粗品精制:将上述反应后得到的混合物趁热倒入圆底烧瓶中,并进行下列操作:
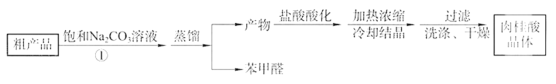
请回答下列问题。
(1)检验粗产品中含有苯甲醛的实验方案是:取粗产品于试管中,加水溶解,滴入NaOH溶液,将溶液调至碱性, _________。
(2)步骤①中肉桂酸与Na2CO3溶液反应的化学方程式是_________。
(3)若最后得到4.81g纯净的肉桂酸,则该反应中肉桂酸的产率是_________。
(4)符合下列条件的肉桂酸的同分异构体有_________种。
i.苯环上含有三个取代基;
ii.该同分异构体遇FeCl3显色且能发生银镜反应。
写出其中任意一种同分异构体的结构简式: _________。