题目内容
16.下列陈述I、Ⅱ正确并且有因果关系的是( )| 选项 | 表述I | 表述II |
| A | SiO2有导电性 | SiO2可用于制备光导纤维 |
| B | SO2有漂白性 | SO2可使溴水褪色 |
| C | 溶液中含有大量的NO3- | 溶液中不能存在大量I-或S2- |
| D | 将淀粉与KCl混合液装于半透膜内,浸泡在盛蒸馏水的烧杯中,5min后取烧杯中液体,加碘水变蓝色 | 半透膜有破损 |
| A. | A | B. | B | C. | C | D. | D |
分析 A、二氧化硅不导电,是制光导纤维的原料;
B、二氧化硫的漂白性是和有色有机物结合为不稳定的无色物质,二氧化硫和溴发生氧化还原反应;
C、硝酸根离子在酸性条件下具有氧化性,中性和碱性条件下不具有氧化性,所以在中性和碱性条件下能存在大量I-或S2-;
D、淀粉是胶体,而胶体不能透过半透膜,加碘水变蓝色,说明半透膜有破损.
解答 解:A、二氧化硅不导电,是制光导纤维的原料,Ⅰ不正确、Ⅱ正确,无因果关系,故A不选;
B、二氧化硫的漂白性是和有色有机物结合为不稳定的无色物质,二氧化硫和溴发生氧化还原反应,Ⅰ、Ⅱ正确但无因果关系,故B不选;
C、硝酸根离子在酸性条件下具有氧化性,中性和碱性条件下不具有氧化性,所以在中性和碱性条件下能存在大量I-或S2-,Ⅰ正确、Ⅱ不正确,无因果关系,故C不选;
D、淀粉是胶体,而胶体不能透过半透膜,加碘水变蓝色,说明半透膜有破损,Ⅰ正确、Ⅱ正确,有因果关系,故D选;
故选:D.
点评 本题考查了二氧化硫、二氧化硅、胶体的性质、硝酸根离子的氧化性的应用,熟练掌握基础是解题关键.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
5.下列四个原电池的有关说法正确的是( )


| A. | 装置①中SO42-的向Al片移动 | |
| B. | 装置②中的Mg片上发生的反应为:2H++2e-═H2↑ | |
| C. | 装置③中铁片被氧化,铜片上产生气体 | |
| D. | 装置④中若有1摩尔铁锈(氧化铁)生成,理论上有4摩尔电子通过导线 |
7.下列对沉淀溶解平衡的描述正确的是( )
| A. | 沉淀溶解达到平衡时,沉淀的速率和溶解的速率相等 | |
| B. | 电解质的溶解开始后,只有电解质的溶解过程,没有电解质的析出过程 | |
| C. | 沉淀溶解达到平衡时,溶液中溶质的各离子浓度相等,且保持不变 | |
| D. | 沉淀溶解达到平衡时,如果再加入难溶性的该沉淀物,将促进溶解 |
4.列有关物质水解的说法不正确的是( )
| A. | 蛋白质水解的最终产物是多肽 | B. | 淀粉水解的最终产物是葡萄糖 | ||
| C. | 纤维素能水解成葡萄糖 | D. | 油脂水解产物之一是甘油 |
1.下列实验操作及现象能够达到实验目的是( )
| 选项 | 实验操作及现象 | 实验目的 |
| A | 溶液中滴加盐酸酸化的氯化钡溶液出现白色沉淀 | 检验溶液中存在SO42- |
| B | FeBr2溶液加入少量氯水,溶液有浅绿色变为黄色 | 比较Fe2+、Br-还原性强弱 |
| C | 向一定浓度Na2SiO3溶液中通CO2,溶液变浑浊 | 比较C、Si非金属性强弱 |
| D | 溶液中加KSCN溶液,再加氯水,观察溶液是否出现血红色 | 检验Fe3+溶液中是否含有Fe2+ |
| A. | A | B. | B | C. | C | D. | D |
8.如图是一氧化碳空气燃料电池的工作原理示意图,a、b均为惰性电极.下列叙述中,不正确的是( )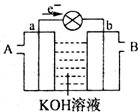

| A. | b电极上发生还原反应 | |
| B. | a电极的电极反应式为:CO+4OH-+2e-═CO32-+2H2O | |
| C. | B处通入的是空气 | |
| D. | 溶液中的K+向b电极方向移动 |
5.从沸腾炉出来的炉气必须净化的原因是( )
| A. | 增加SO2的体积百分比浓度 | |
| B. | 防止矿尘阻塞管道 | |
| C. | 防止催化剂中毒,防止水蒸气跟SO2、SO3结合腐蚀设备 | |
| D. | 炉气中含有的大量N2必须除去 |
6.一定条件下能和氢氧化钠溶液发生反应的是( )
| A. | 汽油 | B. | 色拉油 | C. | 甘油 | D. | 煤油 |