题目内容
1.用N2和CO2 组成的混合气体,其相对于氢气的密度为18,则此混合气体中N2和CO2的物质的量之比为( )| A. | 3:4 | B. | 1:2 | C. | 2:3 | D. | 1:1 |
分析 由相对密度可知,混合气体平均相对分子质量为36,令N2和CO2的物质的量分别为xmol、ymol,根据M=$\frac{{m}_{总}}{{M}_{总}}$列方程计算解答.
解答 解:由相对密度可知,混合气体平均相对分子质量为18×2=36,令N2和CO2的物质的量分别为xmol、ymol,则:$\frac{28x+44y}{x+y}$=36,整理得x:y=1:1,故N2和CO2的体积比(同温同压)为1:1,
故选D.
点评 本题考查物质的量有关计算,难度不大,可以利用十字相乘法进行计算,注对意基础知识的理解掌握.

练习册系列答案
相关题目
11.下列各离子加入强酸或强碱后,都能使其离子浓度降低的是( )
| A. | Al3+ | B. | [Al(OH)4]- | C. | HCO3- | D. | SiO32- |
12.丁香油酚的结构简式为: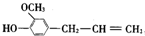 ,下列关于该有机物的说法中,正确的是( )
,下列关于该有机物的说法中,正确的是( )
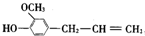 ,下列关于该有机物的说法中,正确的是( )
,下列关于该有机物的说法中,正确的是( )| A. | 丁香油酚的分子式为C10H10O2 | |
| B. | 丁香油酚易溶于水 | |
| C. | 丁香油酚能发生加成反应、加聚反应、取代反应 | |
| D. | 丁香油酚与苯酚互为同系物,可以和碳酸钠反应生成CO2 |
9.mgH2O中含有1mol电子,则m的值为( )
| A. | 18g | B. | 1.8g | C. | 6g | D. | 0.6g |
16.氮化铝(AlN、Al和N的相对原子质量分别为27和14)广泛应用于电子、陶瓷等工业领域.在一定条件下,AlN可通过反应Al2O3+N2+3C$\frac{\underline{\;高温\;}}{\;}$2AlN+3CO合成.下列叙述正确的是( )
| A. | 上述反应中,N2是还原剂,Al2O3是氧化剂 | |
| B. | AlN的摩尔质量为41 g | |
| C. | AlN中氮元素的化合价为+3 | |
| D. | 上述反应中,每生成1 mol AlN需转移3 mol电子 |
6.设阿伏加德罗常数的值为NA,则下列说法不正确的是( )
| A. | 1mol Na参加氧化还原反应时电子转移NA | |
| B. | 3.2g SO2与2.3g NO2所含有的氧原子数相等 | |
| C. | 标准状况下,2.24L SO3含有的O原子数为0.3NA | |
| D. | 1L 0.1mol/LMgCl2溶液中Cl-离子数为0.2NA |
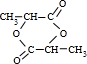
10.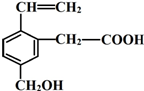 某有机物的结构简式如图,该物质可能有的化学性质是( )
某有机物的结构简式如图,该物质可能有的化学性质是( )
①可燃烧;
②可跟溴加成;
③可使酸性KMnO4溶液褪色;
④可跟NaHCO3溶液反应;
⑤可跟NaOH溶液反应;
⑥1mol该有机物与足量Na反应生成1mol H2.
 某有机物的结构简式如图,该物质可能有的化学性质是( )
某有机物的结构简式如图,该物质可能有的化学性质是( )①可燃烧;
②可跟溴加成;
③可使酸性KMnO4溶液褪色;
④可跟NaHCO3溶液反应;
⑤可跟NaOH溶液反应;
⑥1mol该有机物与足量Na反应生成1mol H2.
| A. | ①②③⑥ | B. | ①②④⑤ | C. | ①②③④⑤ | D. | 全部 |
11.下列关于容量瓶的使用操作中正确的是( )
| A. | 使用容量瓶前应先检查它是否漏水 | |
| B. | 容量瓶先用蒸馏水洗净,再用待配液润洗 | |
| C. | 配制溶液时,如果试样是固体,把称好的试样用纸条小心倒入容量瓶中,缓慢加入蒸馏水到液面距刻度线1~2 cm处,再改用胶头滴管滴加蒸馏水至刻度线 | |
| D. | 浓硫酸稀释后马上转移到容量瓶中 |
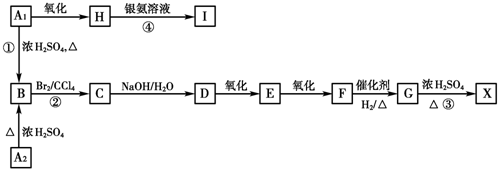
 .
.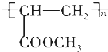 .
.