题目内容
14. 溴主要以Br-形式存在于海水中,海水呈弱碱性.工业上制备的Br2的操作步骤为:
溴主要以Br-形式存在于海水中,海水呈弱碱性.工业上制备的Br2的操作步骤为:①一定条件下,将Cl2通入浓缩的海水中,生成Br2
②利用热空气将Br2吹出,并用浓Na2CO3溶液吸收,生成NaBr、NaBrO3等
③用硫酸酸化步骤②得到的混合物
完成下列填空:
(1)Cl2氧化Br-应在通风橱中酸性 条件下进行,目的是为了避免溴中毒及生成的溴与碱发生反应
(2)Br2可用热空气吹出,其原因是溴的沸点较低,易挥发
(3)写出步骤③所发生的化学反应方程式:3H2SO4+5NaBr+NaBrO3=3Na2SO4+3Br2+3H2O用硫酸而不用盐酸酸化的原因可能是用盐酸酸化,则盐酸被NaBrO3氧化.
(4)为了除去工业Br2中微量的Cl2,可向工业Br2中c
a.通入HBr b.加入Na2CO3溶液 c.加入NaBr溶液 d.加入Na2SO3溶液.
分析 (1)Cl2氧化Br-生成溴单质,通风橱进行防止溴中毒、溴与碱反应;
(2)溴易挥发;
(3)发生氧化还原反应生成硫酸钠、溴单质、水;盐酸能被溴酸钠氧化,并结合溴挥发来分析;
(4)利用NaBr溶液与Cl2反应,然后分液可除去Cl2.
解答 解:(1)Cl2氧化Br-生成溴单质,则应在通风橱中酸性条件下进行,防止溴中毒及生成的溴与碱发生反应,
故答案为:通风橱中酸性;溴中毒及生成的溴与碱发生反应;
(2)因溴的沸点较低,易挥发,Br2可用热空气吹出,
故答案为:溴的沸点较低,易挥发;
(3)发生氧化还原反应生成硫酸钠、溴单质、水,该反应为3H2SO4+5NaBr+NaBrO3=3Na2SO4+3Br2+3H2O,盐酸能被溴酸钠氧化,则不能利用盐酸酸化,且溴挥发,对大气造成污染,则有时运输到目的地后再酸化,
故答案为:3H2SO4+5NaBr+NaBrO3=3Na2SO4+3Br2+3H2O;用盐酸酸化,则盐酸被NaBrO3氧化;
(4)利用NaBr溶液与Cl2反应,然后分液可除去Cl2,只有c符合,其它选项会引入新的杂质,故答案为:c.
点评 本题考查工业制Br2,考查分析问题解决问题的能力,注意溴易挥发及发生的氧化还原反应为解答的关键,注重环境保护和实验安全.

练习册系列答案
 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案
相关题目
18.某盐的溶液中含有K+、Mg2+、NO3-、SO42-四种离子,若K+的浓度为0.2mol/L,Mg2+的浓度为0.4mol/L,SO42-的浓度为0.3mol/L,则NO3-的浓度为( )
| A. | 0.1mol/L | B. | 0.4mol/L | C. | 0.3mol/L | D. | 0.15mol/L |
5.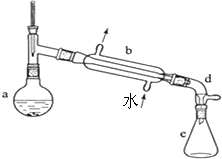 某校实验室合成环己烯的反应和实验装置(夹持及加热部分已省略)如下:
某校实验室合成环己烯的反应和实验装置(夹持及加热部分已省略)如下:
相关数据如下:
实验步骤:
Ⅰ.[合成]:在a中加入20.00g纯环己醇及2小块沸石,冷却搅动下缓慢加入10mL浓硫酸.b中通入冷却水后,缓慢加热a,控制馏出物的温度不超过90℃.
Ⅱ.[提纯]:将反应后粗产物倒入分液漏斗中,依次用少量5% Na2CO3溶液和水洗涤,分离后加入无水CaCl2颗粒,静置一段时间后弃去CaCl2.再进行蒸馏最终获得12.30g纯环己烯.
回答下列问题:
(1)装置b的名称是直形冷凝管.加入沸石的目的是防止混合液爆沸.
(2)本实验分液所得产物应从上口倒出(填“上口”或“下口”).
(3)提纯过程中加入Na2CO3溶液的目的是除去多余的H2SO4,加入无水CaCl2的作用是干燥所得环己烯(产物).
(4)本实验所得环己烯的产率是75%(产率=$\frac{实际产量}{理论产量}$×100%)
 某校实验室合成环己烯的反应和实验装置(夹持及加热部分已省略)如下:
某校实验室合成环己烯的反应和实验装置(夹持及加热部分已省略)如下:
相关数据如下:
| 相对分子质量 | 密度/(g•cm-3) | 沸点/℃ | 溶解性 | |
| 环已醇 | 100 | 0.9618 | 161 | 微溶于水 |
| 环已烯 | 82 | 0.8102 | 83 | 难溶于水 |
Ⅰ.[合成]:在a中加入20.00g纯环己醇及2小块沸石,冷却搅动下缓慢加入10mL浓硫酸.b中通入冷却水后,缓慢加热a,控制馏出物的温度不超过90℃.
Ⅱ.[提纯]:将反应后粗产物倒入分液漏斗中,依次用少量5% Na2CO3溶液和水洗涤,分离后加入无水CaCl2颗粒,静置一段时间后弃去CaCl2.再进行蒸馏最终获得12.30g纯环己烯.
回答下列问题:
(1)装置b的名称是直形冷凝管.加入沸石的目的是防止混合液爆沸.
(2)本实验分液所得产物应从上口倒出(填“上口”或“下口”).
(3)提纯过程中加入Na2CO3溶液的目的是除去多余的H2SO4,加入无水CaCl2的作用是干燥所得环己烯(产物).
(4)本实验所得环己烯的产率是75%(产率=$\frac{实际产量}{理论产量}$×100%)
2. 甲醇是重要的化工原料,在日常生活中有着广泛的应用.
甲醇是重要的化工原料,在日常生活中有着广泛的应用.
工业上一般采用下列反应合成甲醇:CO(g)+2H2(g)?CH3OH(g)△H1
下表所列数据是以上反应在不同温度下的化学平衡常数的数值:
(1)Ⅰ、在一密闭容器中发生反应并达到平衡后,保持其他条件不变,对容器升温,此反应的化学反应平衡应逆向移动(填“正向”、“逆向”、“不”)
Ⅱ、某温度下,将1mol CO和4mol H2充入2L的密闭容器中,充分反应达到平衡后,测得c(CO)=0.1mol/L,则CO的转化率为80%,此时的温度>250℃(填“>”、“<”、“=”)
(2)已知在常温常压下:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l)△H1=-Q1kJ/mol
②2CO (g)+O2(g)=2CO2(g)△H2=-Q2 kJ/mol
③H2O(g)=H2O(l)△H3=-Q3 kJ/mol
请写出甲醇发生不完全燃烧生成一氧化碳和气态水的热化学反应方程式:CH3OH(l)+O2(g)=CO(g)+2H2O(g)△H=-(0.5Q1-0.5Q2-2Q3)kJ/mol
(3)某同学依据甲醇燃烧的反应原理,设计如右图所示的电池装置,工作一段时间后,测得溶液的pH将降低(填“升高”、“降低”、“不变”),该燃料电池负极反应的离子方程式为:CH3OH-6e-+8OH-═CO32-+6H2O.
 甲醇是重要的化工原料,在日常生活中有着广泛的应用.
甲醇是重要的化工原料,在日常生活中有着广泛的应用.工业上一般采用下列反应合成甲醇:CO(g)+2H2(g)?CH3OH(g)△H1
下表所列数据是以上反应在不同温度下的化学平衡常数的数值:
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
Ⅱ、某温度下,将1mol CO和4mol H2充入2L的密闭容器中,充分反应达到平衡后,测得c(CO)=0.1mol/L,则CO的转化率为80%,此时的温度>250℃(填“>”、“<”、“=”)
(2)已知在常温常压下:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l)△H1=-Q1kJ/mol
②2CO (g)+O2(g)=2CO2(g)△H2=-Q2 kJ/mol
③H2O(g)=H2O(l)△H3=-Q3 kJ/mol
请写出甲醇发生不完全燃烧生成一氧化碳和气态水的热化学反应方程式:CH3OH(l)+O2(g)=CO(g)+2H2O(g)△H=-(0.5Q1-0.5Q2-2Q3)kJ/mol
(3)某同学依据甲醇燃烧的反应原理,设计如右图所示的电池装置,工作一段时间后,测得溶液的pH将降低(填“升高”、“降低”、“不变”),该燃料电池负极反应的离子方程式为:CH3OH-6e-+8OH-═CO32-+6H2O.
19.己知:NH3•H2O(aq)与H2SO4(aq)反应生成1mol正盐的△H=-24.2kJ/mol;强酸、强碱的稀溶液反应的中和热的△H=-57.3kJ/mol.则NH3•H2O在水溶液中电离的△H等于( )
| A. | -69.4 kJ/mol | B. | -45.2kJ/mol | C. | +69.4 kJ/mol | D. | +45.2 kJ/mol |
3.室温下向10mL pH=3的醋酸溶液中加入水稀释后,下列说法正确的是( )
| A. | 再加入10mL pH=11 NaOH溶液,混合液pH=7 | |
| B. | 醋酸的电离程度增大,c(H+)亦增大 | |
| C. | 溶液中导电粒子的数目增加,导电性增强 | |
| D. | 溶液中$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)•(O{H}^{-})}$不变 |
4.下列各项中,由实验事实能得出相应结论的是( )
| 选项 | 理由 | 结论 |
| A | 相同物质的量浓度溶液的pH: Ca(ClO)2>CH3COONa | 酸性:CH3COOH>HClO |
| B | 同体积相同pH的盐酸和醋酸与相同的锌 反应的速率:醋酸>盐酸 | 酸性:HCl>CH3COOH |
| C | 相同条件下的沸点: H2O>NH3 | 非金属性:O>N |
| D | 相同物质的量得到电子的数目: 稀硝酸>浓硝酸 | 氧化性:稀硝酸>浓硝酸 |
| A. | A | B. | B | C. | C | D. | D |
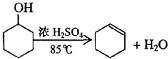
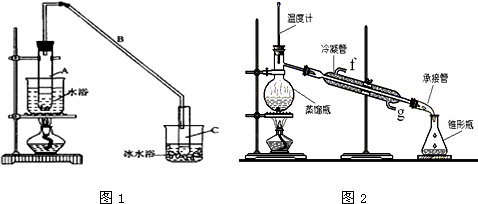
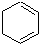 ),试写出该两步反应对应的化学方程
),试写出该两步反应对应的化学方程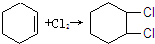 ;
; .
.