��Ŀ����
16��������㶨���ܱ������У�һ������SO2��1.100mol O2�ڴ��������¼��ȵ�600�淢����Ӧ��2SO2+O2$?_{����}^{����}$2SO3���÷�ӦΪ���ȷ�Ӧ������������ʵ�������0.315molʱ��Ӧ�ﵽƽ�⣬����ͬ���¶��²������ѹǿΪ��Ӧǰ��82.5%�������й�������ȷ���ǣ�������| A�� | ��SO3������������SO2�������������ʱ��Ӧ�ﵽƽ�� | |
| B�� | �����¶ȣ�����Ӧ���ʼ�С�����淴Ӧ�������� | |
| C�� | ��ƽ��������ͨ�����BaCl2��Һ�У��õ�����������Ϊ161.980 g | |
| D�� | �ﵽƽ��ʱ��SO2��ת������90% |
���� A��SO3������������SO2���������ʾ���ʾ����Ӧ���ʣ���Ӧʼ�հ��ñ�����ϵ���У�
B�������¶ȣ������淴Ӧ���ʶ���С��
C�������������ʼ���ʵ�����xmol��ƽ��ʱת���Ķ�������Ϊymol����
2SO2��g��+O2��g��?2SO3��g��
��ʼ����mol����x 1.1 0
ת������mol����y 0.5y y
ƽ������mol����x-y 1.1-0.5y y
���������ʵ�������0.315molʱ��Ӧ�ﵽƽ�⣬��0.5y=0.315����y=0.63��
����ͬ���¶��²������ѹǿΪ��Ӧǰ��82.5%����$\frac{x+1.1-0.315}{x+1.1}$=82.5%����x=0.7��
���������ͨ��������Ȼ�����Һ�У�����������Ȼ�����Һ��Ӧ�������ᱵ����������������������ˮ��Ӧ�������ᣬ�������Ȼ�����Ӧ�������ᱵ������0.7mol����������ȫת������0.35mol������������ʣ�࣬������Ԫ���غ�������ᱵ������
D���ﵽƽ��ʱ��SO2��ת����=$\frac{ת���Ķ����������ʵ���}{����������ʼ���ʵ���}$��100%��
��� �⣺A��SO3������������SO2���������ʾ���ʾ����Ӧ���ʣ���Ӧʼ�հ��ñ�����ϵ���У�Ӧ�ǵ�SO3������������SO2�������������ʱ��Ӧ�ﵽƽ�⣬��A����
B�������¶ȣ������淴Ӧ���ʶ���С����B����
C�������������ʼ���ʵ�����xmol��ƽ��ʱת���Ķ�������Ϊymol����
2SO2��g��+O2��g��?2SO3��g��
��ʼ����mol����x 1.1 0
ת������mol����y 0.5y y
ƽ������mol����x-y 1.1-0.5y y
���������ʵ�������0.315molʱ��Ӧ�ﵽƽ�⣬��0.5y=0.315����y=0.63��
����ͬ���¶��²������ѹǿΪ��Ӧǰ��82.5%����$\frac{x+1.1-0.315}{x+1.1}$=82.5%����x=0.7��
���������ͨ��������Ȼ�����Һ�У�����������Ȼ�����Һ��Ӧ�������ᱵ����������������������ˮ��Ӧ�������ᣬ�������Ȼ�����Ӧ�������ᱵ������0.7mol����������ȫת������0.35mol������������ʣ�࣬������Ԫ���غ㣬���ᱵ�����ʵ�����0.7mol����������Ϊ0.7mol��233g/mol=163.1g����C����
D���ﵽƽ��ʱ��SO2��ת����=$\frac{0.63mol}{0.7mol}$��100%=90%����D��ȷ��
��ѡ��D��
���� ���⿼���˻�ѧƽ��ƽ����㡢ƽ��״̬�жϡ���Ӧ����Ӱ�����صȣ�Cѡ��Ϊ�״��㣬ѧ������������������Ȼ�����Һ��Ӧ�������ᱵ����������������Ȼ�����Һ����Ӧ���������������¶���������������ˮ��Ӧ�������ᣬ�������Ȼ�����Ӧ�������ᱵ������

��֪��
�ٻ���������Cl2��Ӧ����PCl3�������Cl2��Ӧ����PCl5��
��PCl3��ˮ��ǿ��ˮ������ H3PO3��HC1��
��PCl3��O2������POCl3��POCl3����PCl3��
��PCl3��POCl3���۷е���±���
| ���� | �۵�/�� | �е�/�� |
| PCl3 | -112 | 75.5 |
| POCl3 | 2 | 105.3 |
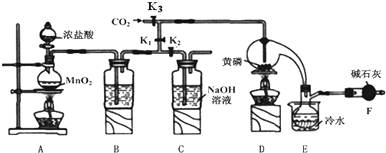
��1��Aװ���������������ӷ���ʽΪMnO2+4H++2Cl-$\frac{\underline{\;\;��\;\;}}{\;}$Mn2++Cl2��+2H2O
��2��B����װ�Լ������ն������������ֹ�����е�H2O������ƿ��PCl3��Ӧ
��3��ʵ�����ʱ����������C�е��Լ����ն����������C�з�Ӧ�����ӷ���ʽΪCl2+2OH-=Cl-+ClO-+2H2O��
��4��F�м�ʯ�ҵ����������ն���������ֹ��Ⱦ��������ֹ�����е�ˮ����������ƿ����PCl3��Ӧ
��5��ʵ��ʱ�����װ�������Ժ��ȴ�K3ͨ������CO2����Ѹ�ټ�����ף�ͨ����CO2���������ž�װ���еĿ�������ֹ������ȼ��
��6���ֲ�Ʒ�г�����POCl3��PCl5�ȣ���������ȳ�ȥPCl5��ͨ��������ʵ��������ƣ������ɵõ��ϴ�����PCl3��
��7��ͨ�����淽���ɲⶨ��Ʒ��PCl3����������
��Ѹ�ٳ�ȡ1.00g��Ʒ����ˮ��Ӧ�����250mL��Һ��
��ȡ������Һ25.00mL�������м���10.00mL 0.1000mol/L��ˮ����ַ�Ӧ��
�����������Һ�м��뼸�ε�����Һ����0.1000mol/L��Na2S2O3��Һ�ζ���
���ظ��ڡ��۲���ƽ������Na2S2O3��Һ8.40mL��
��֪��H3PO3+H2O+I2�TH3PO4+2HI��I2+2Na2S2O3�T2NaI+Na2S4O6������ⶨ������û��������Ӧ�������������ݣ��ò�Ʒ��PC13����������Ϊ79.75%��
��1���жϷ�Ӧ�ﵽƽ��״̬�������ǣ�����ĸ��ţ���ͬ��CD��
A������CH3OH������������CO���������
B�����������ܶȲ���
C�������������ƽ��������������
D��CH3OH��CO��H2��Ũ�ȶ����ٷ����仯
��2���±����������Ƿ�Ӧ�ڲ�ͬ�¶��µĻ�ѧƽ�ⳣ����K����
| �¶� | 250�� | 300�� | 350�� |
| K | 2.041 | 0.270 | 0.012 |
��ij�¶��£���2molCO��6mol H2����2L���ܱ������У���ַ�Ӧ�ﵽƽ��ʱ���c��CO��=0.2mol/L����CO��ת����Ϊ80%����ʱ���¶�Ϊ250�森
��3��Ҫ���CO��ת���ʣ����Բ�ȡ�Ĵ�ʩ��df��
a������b���������c������CO��Ũ��
d������H2��ѹe��������������ѹf��������״�
��4��һ�������£�CO��H2�ڴ���������������5molCH3OH�������仯Ϊ454kJ���ڸ��¶�ʱ�����ݻ���ͬ��3���ܱ������У�����ͬ��ʽͶ�뷴Ӧ����ֺ��¡����ݣ���÷�Ӧ�ﵽƽ��ʱ���й��������£�
| ���� | �� | �� | �� | |
| ��Ӧ��Ͷ���� | 1molCO��2molH2 | 1molCH3OH | 2molCH3OH | |
| ƽ �� ʱ �� �� | CH3OH��Ũ�ȣ�mol/L�� | c1 | c2 | c3 |
| ��Ӧ�������仯 | a kJ | b kJ | c kJ | |
| ��ϵѹǿ��Pa�� | p1 | p2 | p3 | |
| ��Ӧ��ת���� | ��1 | ��2 | ��3 | |
A.2c1��c3 B��a+b��90.8 C.2p2��p3 D����1+��3��1��
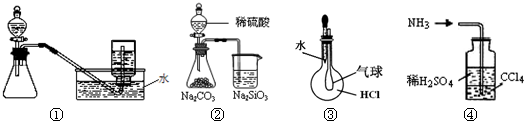
| A�� | ����ͭ��Ũ������ȡ����NO2 | B�� | �ڱȽ�S��C��Si�ķǽ����� | ||
| C�� | ����֤HCl�ܽ��� | D�� | ����������NH3β��������ֹ���� |
 ���ڵ�������Na+��OH�C
���ڵ�������Na+��OH�C ��Һ��������
��Һ��������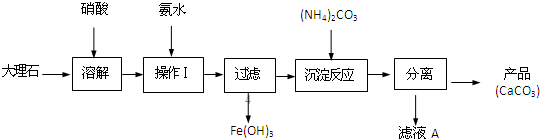
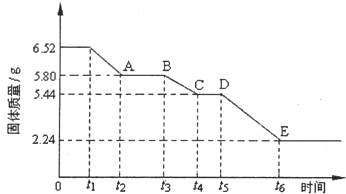
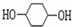 ��·����ͼ��ʾ���밴Ҫ������
��·����ͼ��ʾ���밴Ҫ������
 ��
�� ��F
��F ��
�� ��
�� ��
��