题目内容
【题目】利用如图装置测定中和热的实验步骤如下:
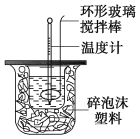
①用量筒量取50 mL 0.25 mol/L硫酸倒入小烧杯中,测出硫酸温度;
②用另一量筒量取50 mL 0.55 mol/L NaOH溶液,并用另一温度计测出其温度;
③将NaOH溶液倒入小烧杯中,设法使之混合均匀,测出混合液最高温度。
回答下列问题:
(1)写出稀硫酸和稀氢氧化钠溶液反应表示中和热的热化学方程式(中和热数值为57.3 kJ/mol): ______。
(2)倒入NaOH溶液的正确操作是________(从下列选出)。
A.沿玻璃棒缓慢倒入 B.分三次少量倒入 C.一次迅速倒入
(3)使硫酸与NaOH溶液混合均匀的正确操作是________(从下列选出)。
A.用温度计小心搅拌 B.揭开硬纸片用玻璃棒搅拌
C.轻轻地振荡烧杯 D.用套在温度计上的环形玻璃棒轻轻地搅动
(4)实验数据如下表:
①请填写下表中的空白:
温度 实验次数 | 起始温度t1℃ | 终止温度t2/℃ | 温度差平均值(t2-t1)/℃ | ||
H2SO4 | NaOH | 平均值 | |||
1 | 26.2 | 26.0 | 26.1 | 29.5 | ____________________ |
2 | 27.0 | 27.4 | 27.2 | 32.3 | |
3 | 25.9 | 25.9 | 25.9 | 29.2 | |
4 | 26.4 | 26.2 | 26.3 | 29.8 | |
②上述实验测量结果得出的中和热的数值与57.3 kJ/mol相比偏小,产生的原因可能是(填字母)_________。
a.实验装置保温、隔热效果差 b.量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
【答案】![]() H2SO4(aq)+NaOH(aq)=
H2SO4(aq)+NaOH(aq)=![]() Na2SO4(aq)+H2O(l)△H=-57.3 kJ/mol C D 3.4 acd
Na2SO4(aq)+H2O(l)△H=-57.3 kJ/mol C D 3.4 acd
【解析】
(1)根据中和热的定义书写热化学方程式;
(2)为防止热量散失,需要将NaOH溶液一次性迅速倒入;
(3)酸和氢氧化钠混合时,用套在温度计上的环形玻璃搅拌棒轻轻地搅动,使硫酸与NaOH溶液混合均匀;
(4)①先判断温度差的有效性,然后求出温度差平均值;
②a. 装置保温、隔热效果差,测得的热量偏小;
b. 量取NaOH溶液的体积时仰视读数,会导致所量的氢氧化钠体积偏大;
c. 分多次把NaOH溶液倒入盛有硫酸的小烧杯中,测得的热量偏小;
d. 温度计测定NaOH溶液起始温度后直接插入稀H2SO4测温度,因发生反应放出部分热量,导致硫酸的起始温度偏高。
(1)中和热是指在稀溶液中,酸与碱发生中和反应生成1 mol H2O时的反应热,其中和热数值为57.3 kJ/mol,则稀硫酸和稀氢氧化钠溶液反应表示中和热的热化学方程式:![]() H2SO4(aq)+NaOH(aq)=
H2SO4(aq)+NaOH(aq)=![]() Na2SO4(aq)+H2O(l)△H=-57.3 kJ/mol,
Na2SO4(aq)+H2O(l)△H=-57.3 kJ/mol,
故答案为![]() H2SO4(aq)+NaOH(aq)=
H2SO4(aq)+NaOH(aq)=![]() Na2SO4(aq)+H2O(l)△H=-57.3 kJ/mol;
Na2SO4(aq)+H2O(l)△H=-57.3 kJ/mol;
(2)中和热测定实验成败的关键是保温工作,沿玻璃棒缓慢倒入或分多次把NaOH溶液倒入盛有硫酸的小烧杯中,热量散失较多,故倒入NaOH溶液的正确操作是一次性迅速倒入,
答案为:C;
(3)使硫酸与NaOH溶液混合均匀的正确操作方法是:用套在温度计上的环形玻璃搅拌棒轻轻地搅动,
故答案为D;
(4)①因第2组数值差别大,误差大,所以数据无效,不可取,则温度差平均值 = ![]() = 3.4,
= 3.4,
故答案为3.4;
②a. 装置保温、隔热效果差,测得的热量偏小,中和热的数值偏小,故a正确;
b. 量取NaOH溶液的体积时仰视读数,会导致所量的氢氧化钠体积偏大,NaOH仍稍过量,确保硫酸完全反应,故b错误;
c. 尽量一次快速将NaOH溶液倒入盛有硫酸的小烧杯中,不允许分多次把NaOH溶液倒入盛有硫酸的小烧杯中,分多次倒入NaOH溶液,热量损失较多,所测中和热的数值偏小,故c正确;
d. 温度计测定NaOH溶液起始温度后直接插入稀H2SO4测温度,硫酸的起始温度偏高,测得的热量偏小,中和热的数值偏小,故d正确。
故答案为acd。

 阅读快车系列答案
阅读快车系列答案