题目内容
9.如表中评价合理的是( )| 选项 | 化学反应及其离子方程式 | 评价 |
| A | 铁与稀盐酸反应: 2Fe+6H+═2Fe3++3H2↑ | 正确 |
| B | 大理石溶于醋酸的反应: CaCO3+2H+═Ca2++CO2↑+H2O | 错误,醋酸应写为分子形式CH3COOH,CaCO3应写成离子形式 |
| C | FeCl3溶液“腐蚀”铜箔: Fe3++Cu═Fe2++Cu2+ | 正确 |
| D | NH4HCO3溶液与过量NaOH浓溶液共热:NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O | 错误,HCO3-也可以与OH-反应 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.铁与盐酸反应生成亚铁离子,不是生成铁离子;
B.大理石和醋酸都需要保留化学式;
C.离子方程式两边正电荷不相等,违反了电荷守恒;
D.氢氧化钠过量,碳酸氢根离子也参与反应.
解答 解:A.铁与稀盐酸反应生成氯化亚铁,正确的离子方程式为:Fe+2H+═Fe2++H2↑,提供的离子方程式错误,评价不合理,故A错误;
B.大理石溶于醋酸的反应,碳酸钙和醋酸都不能拆开,正确的离子方程式为:CaCO3+2CH3COOH=Ca2++H2O+CO2↑+2CH3COO-,题中评价不合理,故B错误;
C.FeCl3溶液“腐蚀”铜箔,二者反应生成氯化亚铁和硫化铜,正确的离子方程式为:2Fe3++Cu═2Fe2++Cu2+,题中离子方程式错误,评价不合理,故C错误;
D.NH4HCO3溶液与过量KOH浓溶液共热,氢氧化钾过量,题中漏掉了碳酸氢根离子的反应,正确的离子方程式为:2OH-+NH4++HCO3-$\frac{\underline{\;\;△\;\;}}{\;}$CO32-+NH3↑+2H2O,该评价合理,故D正确;
故选D.
点评 本题考查了离子方程式的正误判断,题目难度中等,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法,本题解答的关键是判断评价是否合理,不是判断离子方程式是否正确,为易错点.

练习册系列答案
 优等生题库系列答案
优等生题库系列答案 53天天练系列答案
53天天练系列答案
相关题目
19.在恒容密闭容器中发生反应2SO2+O2?2SO3,当其他条件不变时,只改变一个条件,不能加快化学反应速率的是( )
| A. | 增加SO2的浓度 | B. | 充入一定量惰性气体 | ||
| C. | 升高温度 | D. | 使用催化剂 |
17.如图是恒温下某反应的化学反应速率随反应时间变化的示意图.下列叙述与示意图不相符合的是( )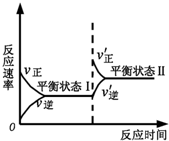

| A. | 反应达平衡时,正反应速率和逆反应速率相等 | |
| B. | 该反应达到平衡状态Ⅰ后,减小反应物浓度,平衡发生移动,达到平衡状态Ⅱ | |
| C. | 该反应达到平衡状态Ⅰ后,增大反应物浓度,平衡发生移动,达到平衡状态Ⅱ | |
| D. | 同一种反应物在平衡状态Ⅰ和平衡状态Ⅱ时浓度不相等 |
14.NA为阿伏伽德罗常数的值.下列叙述正确的是( )
| A. | 常温下,2LpH=12的氨水中含有OH-数目为0.02NA | |
| B. | 氯碱工业中,外电路中转移电子数为0.3NA时产生气体体积(标准状况)为4.48L | |
| C. | 标准状况下,11.2LCH3Cl中非极性共价键数目等于2.0NA | |
| D. | 一定条件下,1molI2和0.2molH2混合充分反应,转移的电子数为0.4NA |
1.磷矿石主要以碳酸钙[Ca3(PO4)2•H2O]和磷灰石[Ca5F(PO4)3]等形式存在.目前国际上磷矿石利用大致有湿法磷酸和热法磷酸两种工艺.其中湿法磷酸是指磷酸矿石用过量硫酸分解制备磷酸.热法磷酸指用过量焦炭、二氧化硅与磷灰石在高温下获得单质磷,然后再由磷制备磷酸.
部分物质的相关性质如下:
(1)以磷矿石为原料,湿法磷酸过程中Ca5F(PO4)3反应的化学方程式为Ca5F(PO4)3+5H2SO4=3H3PO4+5CaSO4+HF↑.现有1吨折合含有五氧化二磷约30%的磷灰石,最多可制得到70%的商品磷酸0.59吨.
(2)热法生产磷酸反应过程中产生大量炉渣和尾气,其中炉渣的主要成分是:CaSiO3(填化学式).尾气中主要含有SiF4、CO(均填化学式).还含有少量PH3、H2S和HF等.将其通入纯碱溶液中可除去气体SiF4、H2S和HF,再通入NaClO溶液可除去具有还原性的PH3气体,写出该反应的离子方程式2PH3+3ClO-=2P+3Cl-+3H2O.
部分物质的相关性质如下:
| 熔点/℃ | 沸点/℃ | 备注 | |
| 白磷 | 44 | 280.5 | |
| PH3 | -133.8 | -87.8 | 难溶于水、有还原性 |
| SiF4 | -90 | -86 | 易水解 |
(2)热法生产磷酸反应过程中产生大量炉渣和尾气,其中炉渣的主要成分是:CaSiO3(填化学式).尾气中主要含有SiF4、CO(均填化学式).还含有少量PH3、H2S和HF等.将其通入纯碱溶液中可除去气体SiF4、H2S和HF,再通入NaClO溶液可除去具有还原性的PH3气体,写出该反应的离子方程式2PH3+3ClO-=2P+3Cl-+3H2O.
18.用铝热法还原下列化合物,当各制得1mol金属单质时,消耗铝的质量最少的是( )
| A. | CO3O4 | B. | WO3 | C. | MnO2 | D. | Cr2O3 |
19.下列说法不正确的是( )
| A. | 有机化学实验中需要用温度计的有石油分馏、硝基苯的制备和乙烯的制取 | |
| B. | 用溴水可以鉴别苯酚溶液、甲苯、乙醇和苯乙烯 | |
| C. | 用酒精可以处理粘在皮肤上的苯酚或苯酚醛树脂制备实验后的试管 | |
| D. | 取适量卤代烃水解后产物,直接滴加AgNO3溶液以确定卤原子种类 |
 .
.