��Ŀ����
����Ŀ��ijЩ�л����ʵķ���ʽ��ȡ�ʵ����λ���㣮���м����д�����ǣ� ��
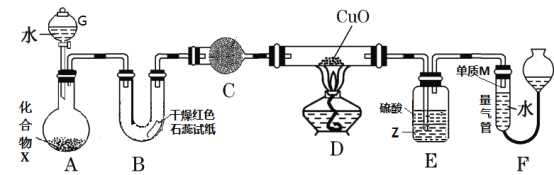
A. �������ļ��顢��ϩ����Ȳ���ȼ�գ����ĵ����������ʵ�����������
B. Wg�����dz��ȼ�պ�ȼ�ղ��ᆳ��������Na2O2��ַ�Ӧ��������������Wg
C. �����������״��ϩ���������������������Ϊa����̼������������![]()
D. �����ʵ������Ҵ����ϩ��![]() ���ȼ�գ����ĵ����������ʵ�����ͬ
���ȼ�գ����ĵ����������ʵ�����ͬ
���𰸡�A
��������
A�����顢��ϩ����Ȳ����������ͨʽΪCxHy������������ȼ���ж����������������Խ�CxHy����CHy/x��y/xԽ������Խ�࣬��������ת���ɵ���ʽΪCH4��CH2��CH���������������������������μ��٣���A˵������
B�������ǵķ���ʽΪC6H12O6�����Բ�д��(CO)6��(H2)6����CO��Na2O2=Na2CO3��H2��Na2O2=2NaOH�����ӵĹ���������CO��H2����������˹����������ӵ��������ǵ���������������������Wg����B˵����ȷ��
C������ķ���ʽΪC2H4O2����ϩ����ͨʽΪCnH2n���û������Կ���(CH2)n��(O2)m�����CH2����������Ϊ(1��a)������![]() �����C%=
�����C%=![]() (1��a)����C˵����ȷ��
(1��a)����C˵����ȷ��
D�����ĺ���������ķ���ʽΪCxHyOz��ȼ�շ���ʽΪCxHyOz��(x��y/4��z/2)O2��xCO2��y/2H2O���Ҵ�����ʽΪC2H6O����ϩ��ķ���ʽΪC3H4O2��1mol�Ҵ��ͱ�ϩ�ᣬ�������������ʵ���Ϊ3mol��3mol����D˵����ȷ��
��ѡA��

����Ŀ�����¶�T1��T2ʱ���ֱ�0.50 mol CH4��1.20 mol NO2�������Ϊ1 L���ܱ����������������·�Ӧ��CH4(g)��2NO2(g)![]() N2(g)��CO2(g)��2H2O(g)�����n(CH4)��ʱ��仯�������±���
N2(g)��CO2(g)��2H2O(g)�����n(CH4)��ʱ��仯�������±���
ʱ��/min | 0 | 10 | 20 | 40 | 50 | |
T1 | n(CH4)/mol | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
T2 | n(CH4)/mol | 0.50 | 0.30 | 0.18 | ���� | 0.15 |
����˵����ȷ����(����)
A. T1ʱ0��10 min NO2��ƽ����Ӧ����Ϊ0.15 mol��L-1��min -1
B. T2ʱCH4��ƽ��ת����Ϊ70.0%
C. ���������������䣬T1ʱ��ƽ����ϵ���ٳ���0.30 mol CH4��0.80 mol H2O(g)��ƽ��������Ӧ�����ƶ�
D. ���������������䣬T1ʱ��ƽ����ϵ���ٳ���0.50 mol CH4��1.20 mol NO2����ԭƽ����ȣ�����ƽ��ʱN2��Ũ������