题目内容
1.氧化还原反应中除了原子守恒(质量守恒)外,氧化剂得电子总数和还原剂失电子总数相等(得失电子守恒).在一定条件下,RO3n-和I-发生反应的离子方程式为:RO3n-+6I-+6H+=R-+3I2+3H2O(R为主族元素)则R元素原子的最外层电子数为( )
| A. | 1 | B. | 3 | C. | 5 | D. | 7 |
分析 根据生成R-离子可知R得1个电子后达到8电子稳定结构,应为第ⅤⅡA族元素,据此判断;
解答 解:RO3n-中R元素的化合价不一定为最高正价,应根据反应物中R-离子的化合价进行判断,根据生成R-离子可知R得1个电子后达到8电子稳定结构,应为第ⅤⅡA族元素,最外层电子数为7,故选:D.
点评 本题考查根据化学式判断化合价,本题用到离子方程式电荷守恒以及离子化合价的判断等问题,本题难度不大,做题时注意“RO3n-中R元素的化合价不一定为最高正价”.

练习册系列答案
 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案
相关题目
11.某气态烃1mol 恰好与2mol HCl加成,生成物分子中的氢又可被6mol Cl2取代,则此气态烃可能是( )
| A. | C2H2 | B. | C2H4 | C. | CH≡C-CH3 | D. | CH2=C(CH3)2 |
12.如表列出了①~⑨九种元素在周期表中的位置:
请按要求回答下列问题.
(1)元素④在周期表中所处位置第二周期ⅥA族⑤、⑥、⑦三种元素形成的离子,离子半径由大到小的顺序是P3->S2->Na+.
(2)按气态氢化物的稳定性由弱到强的顺序排列,⑥④⑦的氢化物稳定性:PH3<H2S<H2O(写氢化物的化学式).
(3)元素⑦的原子结构示意图是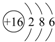 .
.
(4)用电子式表示①与⑨反应得到的化合物的形成过程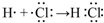 .
.
| ⅠA | ⅧA | |||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | ⑧ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑨ | ||||
(1)元素④在周期表中所处位置第二周期ⅥA族⑤、⑥、⑦三种元素形成的离子,离子半径由大到小的顺序是P3->S2->Na+.
(2)按气态氢化物的稳定性由弱到强的顺序排列,⑥④⑦的氢化物稳定性:PH3<H2S<H2O(写氢化物的化学式).
(3)元素⑦的原子结构示意图是
 .
.(4)用电子式表示①与⑨反应得到的化合物的形成过程
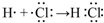 .
.
16.已知:C(s)+O2(g)=CO2(g)△H1
CO2(g)+C(s)=2CO(g)△H2
2CO(g)+O2(g)=2CO2(g)△H3
4Fe(s)+3O2(g)=2Fe2O3(s)△H4
3CO(g)+Fe2O3(s)=3CO2(g)+2Fe(s)△H5
下列关于上述反应焓变的判断正确的是( )
CO2(g)+C(s)=2CO(g)△H2
2CO(g)+O2(g)=2CO2(g)△H3
4Fe(s)+3O2(g)=2Fe2O3(s)△H4
3CO(g)+Fe2O3(s)=3CO2(g)+2Fe(s)△H5
下列关于上述反应焓变的判断正确的是( )
| A. | △H1>0,△H3<0 | B. | △H2>0,△H4>0 | C. | △H2=△H1+△H3 | D. | △H3=$\frac{V{H}_{4}+2V{H}_{5}}{3}$ |
6.如图是198K时N2与H2反应过程中能量变化的曲线图.下列叙述正确的是 ( )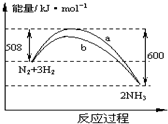

| A. | 该反应的热化学方程式为:N2+3H2?2NH3△H=-92 kJ•mol-1 | |
| B. | 加入催化剂,该化学反应的反应热改变 | |
| C. | b曲线是加入催化剂时的能量变化曲线 | |
| D. | 加入催化剂可增大正反应速率,降低逆反应速率 |
13.有四种短周期元素,它们的结构、性质等信息如下表所述:
请根据表中信息填写:
(1)X元素在周期表中的位置是第二周期第IVA族,其相对分子质量最小的气态氢化物的化学式是CH4.
(2)Y离子半径比Z离子的半径大(填“大”或“小”),Y元素的最高价氧化物的水化物和Z元素的最高价氧化物相互反应的离子方程式是:Al2O3+2OH-=2AlO2-+H2O.
(3)X与M两元素的气态氢化物的稳定性更强的是HCl(填化学式),请再举出一个实例比较M与X两元素的非金属性强弱(用化学方程式表示)Na2CO3+2HClO4=2NaClO4+CO2↑+H2O.
| 元素 | 结构、性质等信息 |
| X | 构成有机物的核心元素,该元素的一种氧化物和气态氢化物都是典型的温室气体 |
| Y | 短周期中(除稀有气体外)原子半径最大的元素,该单质液态时可用作核反应堆的传热介质 |
| Z | 与Y同周期,其最高价氧化物的水化物呈两性 |
| M | 海水中除氢、氧元素外含量最多的元素,其单质或化合物也是自来水生产过程中常用的消毒杀菌剂 |
(1)X元素在周期表中的位置是第二周期第IVA族,其相对分子质量最小的气态氢化物的化学式是CH4.
(2)Y离子半径比Z离子的半径大(填“大”或“小”),Y元素的最高价氧化物的水化物和Z元素的最高价氧化物相互反应的离子方程式是:Al2O3+2OH-=2AlO2-+H2O.
(3)X与M两元素的气态氢化物的稳定性更强的是HCl(填化学式),请再举出一个实例比较M与X两元素的非金属性强弱(用化学方程式表示)Na2CO3+2HClO4=2NaClO4+CO2↑+H2O.




