题目内容
20.下列说法中正确的一组是( )| A. | H2和D2互为同位素 | B. |  和 和  互为同分异构体 互为同分异构体 | ||
| C. | H、D、T互称为同素异形体 | D. |  和 和 是同一种物质 是同一种物质 |
分析 质子数相同,而中子数不同的原子,互为同位素;
分子式相同,结构式不同的化合物,互为同分异构体;
分子组成相同,结构相同的物质为同一物质.
解答 解:A.H2和D2都是氢元素形成的单质,互为同素异形体,故A错误;
B.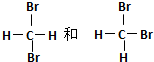 为四面体结构,碳原子连接的原子在空间相邻,组成相同,为同一物质,故B错误;
为四面体结构,碳原子连接的原子在空间相邻,组成相同,为同一物质,故B错误;
C.H、D、T都是氢原子,中子数不同,它们是氢元素的不同核素,互为同位素,故C错误;
D.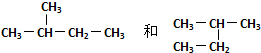 分子组成相同,结构相同,为同一物质,故D正确.
分子组成相同,结构相同,为同一物质,故D正确.
故选D.
点评 本题考查同分异构体与同一物质的区别,难度不大,注意有机物的空间结构.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
11.A元素原子最外层电子数是次外层电子数的3倍,B元素原子次外层是最外层电子数的2倍,则关于A、B元素的判断正确的( )
| A. | A和B元素一定都是第二周期元素 | B. | A和B元素一定是同一主族元素 | ||
| C. | B元素可以是第二周期VIA族元素 | D. | A和B可以相互化合形成化合物 |
8.下列关于化学键的说法正确的是( )
| A. | 由非金属元素组成的化合物不一定是共价化合物 | |
| B. | 非极性键只存在于双原子分子中 | |
| C. | 构成单质分子的微粒一定含有共价键 | |
| D. | 不同元素组成的多原子分子里的化学键一定是极性键 |
15.下列说法不正确的是( )
| A. | H2S、H2O、HF的热稳定性依次增强 | |
| B. | NaOH、KOH、Mg(OH)2的碱性依次减弱 | |
| C. | 在过渡元素中寻找优良的催化剂 | |
| D. | 在周期表中金属元素与非金属元素交界处寻找半导体材料 |
5.下列反应产物中,一定不存在同分异构体的反应是( )
| A. | 异戊二烯( )与等物质的量的Br2发生加成反应 )与等物质的量的Br2发生加成反应 | |
| B. | 丁烷与氯气光照条件下生成的一氯代物 | |
| C. | 甲苯在一定条件下发生硝化生成一硝基甲苯的反应 | |
| D. | 2-丁烯与水的加成反应 |
12.某元素原子M层电子数是K层电子数的3.5倍,则该元素最高价氧化物对应水化物的化学式为( )
| A. | HClO4 | B. | HNO3 | C. | H2SO4 | D. | H3PO4 |
9.向紫色Cr2(SO4)3溶液中加入NaOH溶液至析出蓝灰色沉淀,此时,溶液中存在着如下平衡:Cr3+(紫色)+3OH-?Cr(OH)3(灰蓝色)?CrO2-(绿色)+H++H2O.将上述悬浊液等分为两份,向a试管中加入适量的NaOH溶液,向b试管中加入适量的H2SO4溶液.a、b试管中溶液颜色最终分别为( )
| 选项 | A | B | C | D |
| a试管 | 紫色 | 蓝灰色 | 绿色 | 蓝灰色 |
| b试管 | 绿色 | 绿色 | 紫色 | 紫色 |
| A. | A | B. | B | C. | C | D. | D |
10.下列叙述中正确的是( )
| A. | NH3、CO、CO2都是极性分子 | |
| B. | BF3、SiCl4都是含有极性键的非极性分子 | |
| C. | HF、HCl、HBr、Hl的稳定性依次增强 | |
| D. | CS2、H2O、C2H2都是直线型分子 |