题目内容
9.向紫色Cr2(SO4)3溶液中加入NaOH溶液至析出蓝灰色沉淀,此时,溶液中存在着如下平衡:Cr3+(紫色)+3OH-?Cr(OH)3(灰蓝色)?CrO2-(绿色)+H++H2O.将上述悬浊液等分为两份,向a试管中加入适量的NaOH溶液,向b试管中加入适量的H2SO4溶液.a、b试管中溶液颜色最终分别为( )| 选项 | A | B | C | D |
| a试管 | 紫色 | 蓝灰色 | 绿色 | 蓝灰色 |
| b试管 | 绿色 | 绿色 | 紫色 | 紫色 |
| A. | A | B. | B | C. | C | D. | D |
分析 向a试管中加入适量的NaOH溶液,中和H+,H+浓度降低,平衡右移,溶液中主要含有CrO2-,
向b试管中加入适量的H2SO4溶液,中和OH-,OH-?浓度降低,平衡左移,溶液中主要含有Cr3+.
解答 解:向a试管中加入适量的NaOH溶液,中和H+,H+浓度降低,平衡右移,溶液中主要含有CrO2-,溶液呈绿色;
向b试管中加入适量的H2SO4溶液,中和OH-,OH-?浓度降低,平衡左移,溶液中主要含有Cr3+,溶液呈紫色,
故选C.
点评 本题考查化学平衡的影响因素,难度中等,注意氢氧化铬的酸式电离与碱式电离.

练习册系列答案
相关题目
20.下列说法中正确的一组是( )
| A. | H2和D2互为同位素 | B. |  和 和  互为同分异构体 互为同分异构体 | ||
| C. | H、D、T互称为同素异形体 | D. |  和 和 是同一种物质 是同一种物质 |
4.如图所示装置,将溶液A逐滴加入固体B中,下列叙述中不正确的是( )


| A. | 若a为浓盐酸,b为MnO2,c中盛品红溶液,则c中溶液褪色 | |
| B. | 若a为醋酸溶液,b为贝壳,c中盛过量澄清石灰水,则c中溶液变浑浊 | |
| C. | 若a为浓硫酸,b为Na2SO3固体,c中盛紫色石蕊溶液,则c中溶液变红 | |
| D. | 若a为浓氨水,b为生石灰,c中盛AlCl3溶液,则c中产生白色沉淀 |
14.已知NaHSO4在水中电离方程式为:NaHSO4=Na++H++SO42-.某温度下,向pH=6的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液的pH为2,对于该溶液,下列叙述中不正确的是( )
| A. | 该温度高于25℃ | |
| B. | c(H+)=c(OH-)+c(SO42-) | |
| C. | 水电离出来的c(H+)=1×10-10mol•L-1 | |
| D. | 该温度下加入等体积pH=12的NaOH溶液可使反应后的溶液恰好是中性 |
1.一定条件,在水溶液中物质的量均为1mol的Cl-、ClOx-(x=1,2,3,4)几种微粒的能量(kJ)相对大小与氯元素化合价的相互关系如图所示,下列说法正确的是( )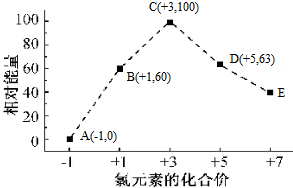

| A. | 所含氯元素的化合价越高,该物质的能量越高 | |
| B. | 所含氯元素的化合价越高,该物质越不稳定 | |
| C. | B→A+D的热化学方程式为3ClO-(aq)=2Cl-(aq)+ClO3-(aq)△H=-117kJ•mol-1 | |
| D. | ClO2-→ClO3-+ClO4-可以自发进行 |
18.化学反应中的能量变化,通常表现为热量的变化,如Ba(OH)2•8H2O 与NH4Cl的反应要吸收热量,在化学上叫作吸热反应.其原因是( )
| A. | 反应物NH4Cl所具有的能量比较低 | |
| B. | 反应物Ba(OH)2•8H2O所具有的能量比较低 | |
| C. | 反应物所具有的总能量高于生成物所具有的总能量 | |
| D. | 反应物所具有的总能量低于生成物所具有的总能量低 |
19.在下列有关晶体的叙述中错误的是( )
| A. | 稀有气体的原子能形成分子晶体 | B. | 离子晶体中,一定存在离子键 | ||
| C. | 原子晶体中,只存在共价键 | D. | 金属晶体的熔沸点均很高 |
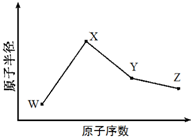 W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如图所示.已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的原子半径在同周期主族元素中最小.
W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如图所示.已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的原子半径在同周期主族元素中最小.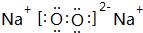 (写化学式);Z的气态氢化物和溴化氢相比,较稳定的是HCl(写化学式).
(写化学式);Z的气态氢化物和溴化氢相比,较稳定的是HCl(写化学式). .
.
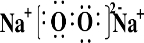 .
.