题目内容
5.现有0.1mol某有机物A在8.96L O2中完全燃烧后,气体体积变为6.72L,通过足量碱石灰吸收后剩余2.24L(气体体积均在标准状况下测定).(1)2.24L剩余气体可能是O2或CO;
(2)若A是烃,其化学式可能是C2H4或C3H6;若A是烃的衍生物,其化学式可能是C2H6O或C3H8O.
分析 n(O2)=$\frac{8.96L}{22.4L/mol}$=0.4mol,燃烧后气体的物质的量为n=$\frac{6.72L}{22.4L/mol}$=0.3mol,通过足量碱石灰吸收后剩余2.24L,即n=$\frac{2.24L}{22.4L/mol}$=0.1mol,如氧气过量,则剩余气体为氧气,如氧气不足,则剩余气体为CO,以此解答该题.
解答 解:(1)通过足量碱石灰吸收后剩余2.24L,如氧气过量,则剩余气体为氧气,如氧气不足,则剩余气体为CO,故答案为:O2;CO;
(2)若A是烃,如氧气过量,则生成二氧化碳为0.3mol-0.1mol=0.2mol,消耗氧气为0.4mol-0.1mol=0.3mol,设烃中H原子数为y,则2+$\frac{y}{4}$=3,y=4,为C2H4,
如氧气不足,燃烧后6.72L气体为二氧化碳和一氧化碳,可知1mol烃含有3molC原子,可能为C3H6或C3H8,方程式为C3Hy+4O2=2CO2+CO+$\frac{y}{2}$H2O,
则y=6,应为C3H6,
若A是烃的衍生物,设其化学式为CxHyOz,
如氧气过量,则生成二氧化碳为0.3mol-0.1mol=0.2mol,消耗氧气为0.4mol-0.1mol=0.3mol,由以上解答可设分子式为C2H4•(H2O)m,m=1符合,为C2H6O,
如氧气不足,燃烧后6.72L气体为二氧化碳和一氧化碳,可知1mol烃含有3molC原子,可设分子式为C3H6•(H2O)n,n=1符合,为C3H8O,
故答案为:C2H4;C3H6;C2H6O;C3H8O.
点评 本题考查有机物分子式的确定,为高频考点,侧重于学生的分析、计算能力的考查,题目难度中等,注意从质量守恒的角度解答该类题目,结合方程式计算.

(已知Ksp[Fe(OH)3]=3.8×10-38; Ksp[Cu(OH)2]=2×10-20;Ksp(ZnS)=1.6×10-24)
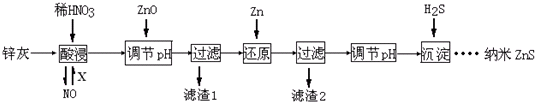
下列说法不正确的是( )
| A. | 酸浸时FeO与稀HNO3反应的离子方程式为3FeO+10H++NO${\;}_{3}^{-}$═3Fe3++NO↑+5H2O | |
| B. | 将酸浸的尾气循环利用,加入的X气体可以是O2 | |
| C. | 滤渣2中的成分和Zn和Fe | |
| D. | 当溶液中Zn2+浓度为小于1.0×10-5mol•L-1时,则可认为其沉淀完全.若要使Zn2+沉淀完全,溶液中S2-浓度应大于1.6×10-19mol•L-1 |
| A. | 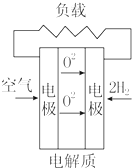 固体氧化物燃料电池 | B. | 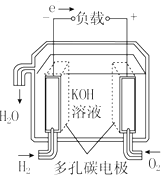 碱性燃料电池 | ||
| C. | 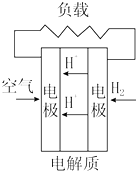 质子交换膜燃料电池 | D. | 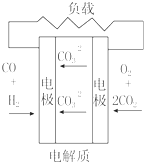 熔融盐燃料电池 |
| A. | FeO | B. | Fe3O4 | ||
| C. | Fe2O3 | D. | Fe3O4 和Fe2O3混合物 |
| A. | 食盐 | B. | 香醋 | C. | 植物油 | D. | 黄酒 |
| A. | 热化学方程式未注明温度和压强时,△H表示标准状况下的数据 | |
| B. | 热化学方程式中各物质前的化学计量数不表示分子个数,只代表物质的量 | |
| C. | 同一化学反应,化学计量数不同,△H不同;化学计量数相同而状态不同,△H也不相同 | |
| D. | 化学反应过程所吸收或放出的热量与参加反应的物质的物质的量成正比 |
| A | ①能使溴的四氯化碳溶液褪色; ②比例模型为  ③能与水在一定条件下反应生成C |
| B | ①由C、H两种元素组成;②球棍模型为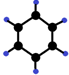 |
| C | ①由C、H、O三种元素组成;②能与Na反应; ③与E反应生成相对分子质量为88的酯 |
| D | ①相对分子质量比C少2;②能由C催化氧化得到 |
| E | ①由C、H、O三种元素组成;②其水溶液能使紫色石蕊试液变红 |
A~E中,属于烃的是AB(填字母).
A能使溴的四氯化碳溶液褪色,发生反应的化学方程式为CH2=CH2+Br2→CH2BrCH2Br.
C催化氧化生成D的化学方程式为2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O.
有机物B具有的性质是②③(填序号).
①无色无味的液体;②有毒;③不溶于水;④密度比水大;⑤能使酸性KMnO4溶液和溴水褪色.

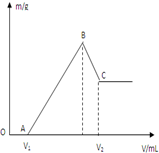 将0.1molMg、Al混合物溶于100mL4mol/L的盐酸中,然后再滴加1mol/L的NaOH溶液,在滴加NaOH溶液的过程中,沉淀质量m与NaOH溶液的体积V的变化如图所示.
将0.1molMg、Al混合物溶于100mL4mol/L的盐酸中,然后再滴加1mol/L的NaOH溶液,在滴加NaOH溶液的过程中,沉淀质量m与NaOH溶液的体积V的变化如图所示.