题目内容
7.NOx是汽车尾气中的主要污染物之一.(1)NOx能形成酸雨,写出NO2转化为HNO3的化学方程式:3NO2+H2O=2HNO3+NO.
(2)汽车发动机工作时会引发N2和O2反应,其能量变化示意图如图:
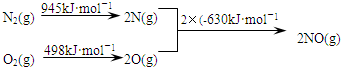
①写出该反应的热化学方程式:N2(g)+O2(g)=2NO(g)△H=+183 kJ•moL-1.
②随温度升高,该反应化学平衡常数的变化趋势是增大..
(3)在汽车尾气系统中装置催化转化器,可有效降低NOX的排放.当尾气中空气不足时,NOX在催化转化器中被还原成N2排出.写出NO被CO还原的化学方程式:2NO+2CO$\frac{\underline{催化剂}}{△}$N2+2CO2.
分析 (1)二氧化氮和水反应生成硝酸和一氧化氮;
(2)①根据能量变化图计算反应热,反应热=吸收的能量-放出的能量,再根据热化学反应方程式的书写规则书写;②温度升高,平衡向吸热方向移动;
(3)NO被CO还原,可生成氮气和二氧化碳.
解答 解:(1)二氧化氮和水反应生成硝酸和一氧化氮,反应方程式为:3NO2+H2O=2HNO3+NO,
故答案为:3NO2+H2O=2HNO3+NO;
(2)①该反应中的反应热=(945+498)kJ/mol-2×630kJ/mol=+183kJ/mol,所以其热化学反应方程式为:N2(g)+O2(g)=2NO(g)△H=+183 kJ•moL-1,
故答案为:N2(g)+O2(g)=2NO(g)△H=+183 kJ•moL-1;
②温度升高,平衡向吸热方向移动,化学平衡常数增大,
故答案为:增大;
(3)由题意可知,NO被CO还原,可生成氮气和二氧化碳,反应的方程式为2NO+2CO$\frac{\underline{催化剂}}{△}$N2+2CO2,
故答案为:2NO+2CO$\frac{\underline{催化剂}}{△}$N2+2CO2.
点评 本题涉及化学反应方程式、热化学反应方程式的书写等知识点,注意反应热的计算方法,为易错点,题目难度不大.

练习册系列答案
相关题目
17.下列表达正确的是( )
| A. | HClO的电子式为 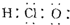 | |
| B. | H2S的电子式可表示为 | |
| C. | 用电子式表示Na2O的形成过程为2Na×+ →2Na+ →2Na+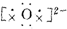 | |
| D. | MgCl2的电子式为 Mg2+ Mg2+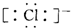 |
18.下列化学用语正确的是( )
| A. | 氯化钙的化学式:CaCl | |
| B. | 镁离子结构示意图: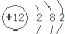 | |
| C. | 碳酸钠的电离方程式:Na2CO3═Na++CO32- | |
| D. | 氢氧化钡的电离方程式Ba(OH)2═Ba2++2OH- |
15.以下符号正确的是( )
| A. | 2d1 | B. | 3f7 | C. | 6s3 | D. | 7p2 |
2.由2-溴丙烷为主要原料制取1,2-丙二醇时,需要经历的反应依次是( )
| A. | 加成→消去→取代 | B. | 消去→加成→取代 | C. | 取代→消去→加成 | D. | 取代→加成→消去 |
12.下列溶液一定呈中性的是( )
| A. | pH=7的溶液 | B. | c(H+)=c(OH)=10-6mol/L溶液 | ||
| C. | 使酚酞试液呈无色的溶液 | D. | 任何盐溶液 |
19.由1-溴丁烷为主要原料制取1,2-二溴丁烷时,发生的反应依次为( )
| A. | 消去反应、加成反应 | B. | 加成反应,消去反应 | ||
| C. | 取代反应、加成反应 | D. | 加成反应、取代反应 |
17.下列各组离子,同时符合下列条件的是( )
①在溶液中能大量共存;②加入过量氢氧化钠溶液并加热,既无沉淀又无气体生成.
①在溶液中能大量共存;②加入过量氢氧化钠溶液并加热,既无沉淀又无气体生成.
| A. | H+、HCO3-、Ca2+ | B. | Ba2+、H+、Cl- | C. | Ca2+、NH4+、HCO3- | D. | Mg2+、NH4+、SO42- |