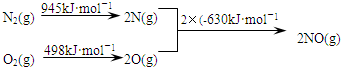题目内容
19.由1-溴丁烷为主要原料制取1,2-二溴丁烷时,发生的反应依次为( )| A. | 消去反应、加成反应 | B. | 加成反应,消去反应 | ||
| C. | 取代反应、加成反应 | D. | 加成反应、取代反应 |
分析 1-溴丁烷在加热条件下和NaOH的醇溶液发生消去反应生成1-丁烯,1-丁烯和溴发生加成反应生成1,2-二溴丁烷,据此分析解答.
解答 解:1-溴丁烷在加热条件下和NaOH的醇溶液发生消去反应生成1-丁烯,反应方程式为Br(CH2)3CH3+NaOH$→_{△}^{醇}$CH2=CHCH2CH3+NaBr,属于消去反应;
1-丁烯和溴发生加成反应生成1,2-二溴丁烷,反应方程式为CH2=CHCH2CH3+Br2→BrCH2CHBrCH2CH3 ,属于加成反应,
故选A.
点评 本题考查有机物结构和性质,为高频考点,明确官能团及其性质关系是解本题关键,知道常见反应类型及反应条件,注意基础知识的总结和归纳,题目难度不大.

练习册系列答案
相关题目
10.下表是元素周期表的一部分,表中序号分别代表某一元素.请回答下列问题.
(1)①~⑩中,金属性最强的元素是Na(写元素符号,下同);非金属性最强的元素是F;形成化合物种类最多的元素是C;某元素的气态氢化物与其最高价氧化物的水化物可直接化合生成一种盐,该元素是N.
(2)③、③、⑤,其原子半径由大到小的顺序是Na>N>F(写元素符号).
(3)⑧、⑨的氢化物,还原性更强的是H2S(填化学式).
(4)①~⑨的最高价氧化物的水化物中:酸性最强的是HClO4(填化学式);碱性最强的是NaOH(填化学式),它的水溶液与⑦的最高价氧化物的水化物反应的离子离子方程式为OH-+Al(OH)3=AlO2-+2H2O.
| 周期/族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅧA | 0 |
| 二 | ① | ② | ③ | ④ | ||||
| 三 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(2)③、③、⑤,其原子半径由大到小的顺序是Na>N>F(写元素符号).
(3)⑧、⑨的氢化物,还原性更强的是H2S(填化学式).
(4)①~⑨的最高价氧化物的水化物中:酸性最强的是HClO4(填化学式);碱性最强的是NaOH(填化学式),它的水溶液与⑦的最高价氧化物的水化物反应的离子离子方程式为OH-+Al(OH)3=AlO2-+2H2O.
4.常温下,有①Na2CO3溶液;②NaHCO溶液;③氨水;④NH4Cl溶液各25mL,其物质的量浓度均为0.1mol.L-1.关于上述四种溶液的说法正确的是( )
| A. | 水的电离程度:①<② | |
| B. | ①、②中粒子浓度关系均符合:c(Na+)+c(H+)=c(OH+)+c(HCO2-)+c(CO32-) | |
| C. | 将③、④混合,所得溶液的pH>7,则该溶液中:c(NH4+)+c(NH3.H2O)<0.1mol.L-1 | |
| D. | 向③、④中分别加入25mL0.1mol.L-1盐酸后,溶液中c(NH4+):③<④ |
11.某无色溶液中存在大量的Ba2+、NH4+、Cl-,该溶液中还可能大量存在的离子是( )
| A. | Fe3+ | B. | CO32- | C. | Mg2+ | D. | OH- |
8.在0.1mol/L CH3COOH溶液中存在如下电离平衡:CH3COOH?CH3COO-+H+,对于该平衡,下列叙述不正确的是( )
| A. | 加入水时,平衡向正反应方向移动,溶液中n(H+)增大 | |
| B. | 加入少量冰醋酸,平衡向正反应方向移动,溶液中c(H+)增大 | |
| C. | 加入少量0.1 mol•L-1 HCl溶液,平衡向逆反应方向移动,溶液中c(H+)减小 | |
| D. | 加入少量CH3COONa固体,平衡向逆反应方向移动,溶液中c(H+)减小 |