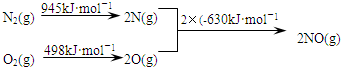题目内容
17.下列各组离子,同时符合下列条件的是( )①在溶液中能大量共存;②加入过量氢氧化钠溶液并加热,既无沉淀又无气体生成.
| A. | H+、HCO3-、Ca2+ | B. | Ba2+、H+、Cl- | C. | Ca2+、NH4+、HCO3- | D. | Mg2+、NH4+、SO42- |
分析 根据离子之间不能结合生成沉淀、气体、水等,则离子大量共存,并结合加入过量氢氧化钠溶液并加热,既无沉淀又无气体生成来解答.
解答 解:A.H+、HCO3-结合生成水和气体,不能大量共存,故A错误;
B.该组离子之间不反应,可大量共存,且加入过量氢氧化钠溶液并加热,既无沉淀又无气体生成,故B正确;
C.该组离子之间不反应,可大量共存,但加入过量氢氧化钠溶液并加热,生成碳酸钙沉淀和氨气,故C错误;
D.该组离子之间不反应,可大量共存,但加入过量氢氧化钠溶液并加热,生成氢氧化镁沉淀和氨气,故D错误;
故选B.
点评 本题考查离子共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重复分解反应的离子共存考查,题目难度不大.

练习册系列答案
相关题目
8.在0.1mol/L CH3COOH溶液中存在如下电离平衡:CH3COOH?CH3COO-+H+,对于该平衡,下列叙述不正确的是( )
| A. | 加入水时,平衡向正反应方向移动,溶液中n(H+)增大 | |
| B. | 加入少量冰醋酸,平衡向正反应方向移动,溶液中c(H+)增大 | |
| C. | 加入少量0.1 mol•L-1 HCl溶液,平衡向逆反应方向移动,溶液中c(H+)减小 | |
| D. | 加入少量CH3COONa固体,平衡向逆反应方向移动,溶液中c(H+)减小 |
12.有两种某植物的营养液,其配方如下表所示.对于两种营养液的成分,下列说法中正确的是( )
| 物质 序号 | KCl | K2SO4 | ZnSO4 | ZnCl2 |
| 1 | 0.3mol | 0.2mol | 0.1mol | - |
| 2 | 0.1mol | 0.3mol | - | 0.1mol |
| A. | 只有c(K+)相同 | B. | 只有c(Cl-)相同 | ||
| C. | 完全相同 | D. | 两种营养液功效不同 |
2.改革开放以来,祖国越来越富强,人民生活水平不断提高,不合理的饮食习惯严重影响身体健康,下列饮食习惯科学的是( )
| A. | 多吃肉,少吃蔬菜水果 | |
| B. | 合理摄入糖类、油脂等,注意膳食平衡 | |
| C. | 为防止变胖,炒菜时不放油 | |
| D. | 多饮用纯净水,少饮用矿泉水 |
6.下列各物质的分类、名称(俗名)、化学式都正确的是( )
| A. | 碱性氧化物 氧化铁 FeO | B. | 酸性氧化物 碳酸气 CO2 | ||
| C. | 酸 硫酸 H2S | D. | 盐 纯碱 NaOH |
10.硼镁泥是一种工业废料,主要成份是MgO(占40%),还有CaO、MnO、Fe2O3、FeO、Al2O3、SiO2等杂质,以此为原料制取的硫酸镁,可用于印染、造纸、医药等工业.从硼镁泥中提取MgSO4•7H2O的工艺流程如下:
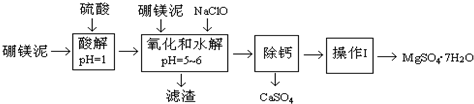
已知:NaClO与Mn2+反应产生MnO2沉淀.
根据题意回答下列问题:
(1)实验中需用1.00mol/L的硫酸80.0mL,若用98%的浓硫酸来配制,除量筒、玻璃棒、烧杯、胶头滴管外,还需要的玻璃仪器是烧杯、100mL容量瓶.
(2)滤渣的主要成份有Fe(OH)3、Al(OH)3、MnO2、SiO2
(3)加入的NaClO可与Mn2+反应产生MnO2沉淀,该反应的离子方程式:Mn2++ClO-+H2O═MnO2↓+2H++Cl-.在调节pH=5-6之前,还有一种离子也会被NaClO氧化,该反应的离子方程式为:2Fe2++ClO-+2H+═2Fe3++Cl-+H2O.
(4)已知MgSO4、CaSO4的溶解度如下表:
“除钙”是将MgSO4和CaSO4混合溶液中的CaSO4除去,根据上表数据,其主要操作过程是蒸发浓缩(结晶),趁热过滤.
(5)如果测得提供的硼镁泥的质量为100.0g,得到的MgSO4•7H2O196.8g,则MgSO4•7H2O的产率为70%(相对分子质量:MgSO4•7H2O-246 MgO-40).

已知:NaClO与Mn2+反应产生MnO2沉淀.
根据题意回答下列问题:
(1)实验中需用1.00mol/L的硫酸80.0mL,若用98%的浓硫酸来配制,除量筒、玻璃棒、烧杯、胶头滴管外,还需要的玻璃仪器是烧杯、100mL容量瓶.
(2)滤渣的主要成份有Fe(OH)3、Al(OH)3、MnO2、SiO2
(3)加入的NaClO可与Mn2+反应产生MnO2沉淀,该反应的离子方程式:Mn2++ClO-+H2O═MnO2↓+2H++Cl-.在调节pH=5-6之前,还有一种离子也会被NaClO氧化,该反应的离子方程式为:2Fe2++ClO-+2H+═2Fe3++Cl-+H2O.
(4)已知MgSO4、CaSO4的溶解度如下表:
| 温度(℃) | 40 | 50 | 60 | 70 |
| MgSO4 | 30.9 | 33.4 | 35.6 | 36.9 |
| CaSO4 | 0.210 | 0.207 | 0.201 | 0.193 |
(5)如果测得提供的硼镁泥的质量为100.0g,得到的MgSO4•7H2O196.8g,则MgSO4•7H2O的产率为70%(相对分子质量:MgSO4•7H2O-246 MgO-40).