题目内容
15.三种主族非金属元素X、Y、Z在周期表中的位置如图所示,则下列说法中错误的是( )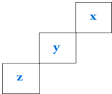
| A. | 元素Z一定是长周期元素,且既有金属性又有非金属性 | |
| B. | 三种元素中X元素的最高价氧化物对应的水化物酸性最强 | |
| C. | 三种元素中X元素的气态氢化物还原性最弱 | |
| D. | Y元素可形成多种不同的单质 |
分析 X、Y、Z是三种非金属主族元素,那么应位于ⅣA~ⅦA族,由元素在周期表中的物质可知,X为F、Y为S、Z为As.
解答 解:X、Y、Z是三种非金属主族元素,那么应位于ⅣA~ⅦA族,由元素在周期表中的物质可知,X为F、Y为S、Z为As,
A、Z为As,处于第四周期第VA族,是长周期,故A正确;
B、X为F,无最高价和含氧酸,故B错误;
C、元素非金属性越强,其对应氢化物还原性越弱,故C正确;
D、S可形成单斜硫、斜方硫等多种单质,故D正确,
故选B.
点评 本题考查元素周期表,侧重金属性与非金属性、气态氢化物还原性等的考查,比较基础,注意对元素周期表的整体把握.

练习册系列答案
 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案 应用题作业本系列答案
应用题作业本系列答案
相关题目
10.下列表示物质结构的化学用语或模型正确的是( )
| A. | 醛基的电子式 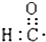 | B. | 丙烷的分子结构的比例模型: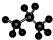 | ||
| C. | 乙烯的最简式(实验式):CH2 | D. | 硝基苯的结构简式: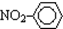 |
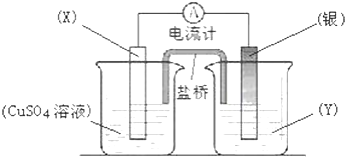
20.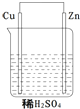 关于如图所示的原电池下列叙述正确的是( )
关于如图所示的原电池下列叙述正确的是( )
①电子由铜流向锌
②正极反应式为Cu+2e-=Cu2+
③SO42-向铜极移动
④铜电极上有气泡
⑤若有0.5mole-流经导线,则可产生0.25molH2
⑥烧杯中溶液的PH升高.
 关于如图所示的原电池下列叙述正确的是( )
关于如图所示的原电池下列叙述正确的是( )①电子由铜流向锌
②正极反应式为Cu+2e-=Cu2+
③SO42-向铜极移动
④铜电极上有气泡
⑤若有0.5mole-流经导线,则可产生0.25molH2
⑥烧杯中溶液的PH升高.
| A. | ①②③ | B. | ④⑤⑥ | C. | ①③⑤ | D. | ②④⑥ |
4.某恒温密闭容器中,可逆反应A(s)?B(?)+C(g)△H=+a kJ/mol达到平衡.缩小容器体积,重新达到平衡时,C(g)的浓度与缩小体积前的平衡浓度相等.以下分析正确的是( )
| A. | 产物B的状态只能为固态或液态 | |
| B. | 平衡时,单位时间内c(A)消耗﹕c(C)消耗=1﹕1 | |
| C. | 保持体积不变,向平衡体系中加入B,平衡可能向逆反应方向移动 | |
| D. | 若开始时向容器中加入1molB和1molC,达到平衡时放出热量a kJ |
5.如图是课外活动小组设计的用化学电源使LED灯发光的装置.下列说法错误的是( )


| A. | 如果将硫酸换成柠檬汁,导线中不会有电子流动 | |
| B. | 装置中存在“化学能→电能→光能”的转换 | |
| C. | 铜片表面有气泡生成 | |
| D. | 如果将锌片换成铁片,电路中的电流方向不变 |