题目内容
10.下列表示物质结构的化学用语或模型正确的是( )| A. | 醛基的电子式 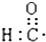 | B. | 丙烷的分子结构的比例模型: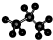 | ||
| C. | 乙烯的最简式(实验式):CH2 | D. | 硝基苯的结构简式: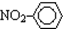 |
分析 A.氧原子最外层有6个电子,氧上的孤对电子没有写出;
B.比例模型突出的是原子之间相等大小以及原子的大致连接顺序、空间结构,不能体现原子之间的成键的情况;
C.最简式指用元素符号表示化合物分子中各元素的原子个数比的最简关系式;
D.硝基苯中苯环应与硝基上的氮原子相连.
解答 解:A.醛基中碳原子与氧原子之间形成2对共用电子对,与氢原子之间形成1对共用电子对,醛基的电子式为 ,故A错误;
,故A错误;
B.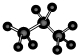 为丙烷的球棍模型,丙烷的比例模型主要体现出其原子的相对体积大小,丙烷正确的比例模型为:
为丙烷的球棍模型,丙烷的比例模型主要体现出其原子的相对体积大小,丙烷正确的比例模型为: ,故B错误;
,故B错误;
C.乙烯的分子式为C2H4,则其最简式为CH2,故C正确;
D.硝基苯化学式为C6H5NO2,硝基苯中苯环应与硝基上的氮原子相连,硝基苯正确的结构简式为: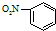 ,故D错误;
,故D错误;
故选C.
点评 本题考查常用化学用语的书写方法,题目难度中等,注意掌握电子式、比例模型与球棍模型、最简式、结构简式的概念及书写原则,试题侧重考查学生的规范答题能力.

练习册系列答案
相关题目
6.下列关于铜-锌-稀硫酸构成的原电池的有关叙述,错误的是( )
| A. | 锌为负极,锌发生氧化反应 | |
| B. | 铜为正极 | |
| C. | 负极发生还原反应,正极发生氧化反应 | |
| D. | 外电路电子流入的一极为正极,电子流出的一极为负极 |
1.几种短周期元素的原子半径及主要化合价见表:
根据表中信息,判断以下说法正确的是( )
| 元素符号 | X | Y | Z | R | T |
| 原子半径(nm) | 0.160 | 0.080 | 0.102 | 0.143 | 0.074 |
| 主要化合价 | +2 | +2 | -2,+4,+6 | +3 | -2 |
| A. | 单质与稀硫酸反应的速率快慢:R>Y>X | |
| B. | 离子半径:T2->X2+ | |
| C. | 元素最高价氧化物的水化物的碱性:Y>R>X | |
| D. | 气态氢化物的稳定性:Z>T |
18.已知2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O.下列关于该反应的说法中正确的是( )
①该反应是一个放热反应
②参加反应的氢气和氧气的总能量高于反应生成的水的总能量
③该反应是一个吸热反应
④参加反应的氢气和氧气的总能量低于反应生成的水的总能量.
①该反应是一个放热反应
②参加反应的氢气和氧气的总能量高于反应生成的水的总能量
③该反应是一个吸热反应
④参加反应的氢气和氧气的总能量低于反应生成的水的总能量.
| A. | ①② | B. | ①④ | C. | ②③ | D. | ③④ |
5.下列各组物质属于同分异构体的是( )
| A. | 丁烷与丁烯 | B. | 乙醇与乙醚 | ||
| C. | 丙醛与丙酮 | D. | 2,2-二甲基丙烷与新戊烷 |
15.三种主族非金属元素X、Y、Z在周期表中的位置如图所示,则下列说法中错误的是( )
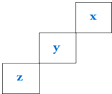

| A. | 元素Z一定是长周期元素,且既有金属性又有非金属性 | |
| B. | 三种元素中X元素的最高价氧化物对应的水化物酸性最强 | |
| C. | 三种元素中X元素的气态氢化物还原性最弱 | |
| D. | Y元素可形成多种不同的单质 |
2.相同条件下,下列各组中的两个反应的焓变前者大于后者的是( )
| A. | H2(g)+Cl2(g)=2HCl(g) 和H2(g)+Cl2(g)=2HCl(aq) | |
| B. | C2H4(g)+H2(g)=C2H6(g)和C3H6(g)+H2(g)=C3H8(g) | |
| C. | 2H2(g)+O2(g)=2H2O(l)和2H2(g)+O2(g)=2H2O(g) | |
| D. | C(s)+O2(g)=CO2(g)和C(s)+$\frac{1}{2}$O2(g)=CO(g) |
19.如图所示2个甲分子反应生成1个丙分子和3个乙分子,下列判断不正确的是( )
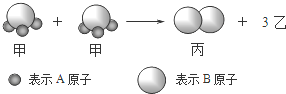

| A. | 1个乙分子中含有2个A原子 | B. | 摩尔质量关系为:2M (甲)=M (乙)+M (丙) | ||
| C. | 该反应一定属于氧化还原反应 | D. | 该反应类型是分解反应 |
20.H、C、N、O、Na、Al、S、Cl Si是常见的元素
(1)C元素位于元素周期表的位置第二周期,第IVA族;C元素的一种同位素可以测定文物年代,这种同位素的符号为14C.
(2)用“>”、“<”或“=”填空
(3)这些元素中属于第三周期元素的是Na、Al、S、Cl、Si
(4)在(3)中元素的非金属性由强到弱的顺序为Cl>S>Si,能证明其递变规律的事实是CD(填字母)
A.氧化物对应水化物的酸性 B.气态氢化物的沸点
C.单质与氢气反应的难易程度 D.氢化物的稳定性
(5)H、C、N、O、Na、Cl 三种元素间可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式: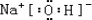 .
.
(1)C元素位于元素周期表的位置第二周期,第IVA族;C元素的一种同位素可以测定文物年代,这种同位素的符号为14C.
(2)用“>”、“<”或“=”填空
| 离子半径 | 酸性 | 还原性 | 得电子能力 |
| N3-> Al3+ | H2SO4< HClO4 | O2-< S2- | 35Cl= 37Cl |
(4)在(3)中元素的非金属性由强到弱的顺序为Cl>S>Si,能证明其递变规律的事实是CD(填字母)
A.氧化物对应水化物的酸性 B.气态氢化物的沸点
C.单质与氢气反应的难易程度 D.氢化物的稳定性
(5)H、C、N、O、Na、Cl 三种元素间可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:
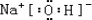 .
.