题目内容
二甲醚(CH3OCH3,沸点为-24.9℃)被称为21世纪的新型能源。科学家利用太阳能分解水生成的氢气与从烟道气中分离出的CO2在催化剂作用下合成二甲醚,并开发出直接以二甲醚为燃料的燃料电池。其合成流程如下:

(1)已知:CH3OCH3(g)、H2(g)的标准燃烧热分别为:△H= -1455.0kJ·mol-1、△H=" -285.8" kJ·mol-1。写出以CO2、H2合成CH3OCH3的热化学方程式: ;
(2)15~20%的乙醇胺(HOCH2CH2NH2)水溶液具有弱碱性,上述合成线路中用作CO2吸收剂。写出吸收CO2反应的化学方程式 ;
(3)一定条件下用CO2和H2合成二甲醚,反应物气流量对CO2的转化率、二甲醚的选择性(是指转化生成二甲醚的碳占已转化碳的比例)影响结果如图1所示,当控制气流量为28mL· min-1时,则生成0.3mol二甲醚需要通入CO2的物质的量为 ;

图1 图2
(4)图2为二甲醚燃料电池示意图。
①a电极的电极反应式为 ;
②若以1.12 L·min-l(标准状况)的速率向该电池中通入二甲醚,用该电池电解50mL2 mol·L-1 CuSO4溶液,通电0.50 min后,计算理论上可析出金属铜的质量为 。

(1)已知:CH3OCH3(g)、H2(g)的标准燃烧热分别为:△H= -1455.0kJ·mol-1、△H=" -285.8" kJ·mol-1。写出以CO2、H2合成CH3OCH3的热化学方程式: ;
(2)15~20%的乙醇胺(HOCH2CH2NH2)水溶液具有弱碱性,上述合成线路中用作CO2吸收剂。写出吸收CO2反应的化学方程式 ;
(3)一定条件下用CO2和H2合成二甲醚,反应物气流量对CO2的转化率、二甲醚的选择性(是指转化生成二甲醚的碳占已转化碳的比例)影响结果如图1所示,当控制气流量为28mL· min-1时,则生成0.3mol二甲醚需要通入CO2的物质的量为 ;

图1 图2
(4)图2为二甲醚燃料电池示意图。
①a电极的电极反应式为 ;
②若以1.12 L·min-l(标准状况)的速率向该电池中通入二甲醚,用该电池电解50mL2 mol·L-1 CuSO4溶液,通电0.50 min后,计算理论上可析出金属铜的质量为 。
(1)
(2)
(3)20mol
(4)① CH3OCH3-12e-+3H2O=2CO2+12H+
② 6.4g (每空2分)

(2)

(3)20mol
(4)① CH3OCH3-12e-+3H2O=2CO2+12H+
② 6.4g (每空2分)
试题分析:(1)已知:CH30CH3(g)、H2(g)的标准燃烧热分别为:△H=-1455.OkJ?mol-1、△H=-285.8kJ?mol-1,①CH30CH3(g)+3O2(g)═2CO2(g)+3H2O(l)△H=-1455.0kJ?mol-1;
②H2(g)+1/2O2(g)═H2O(l)△H=-285.8kJ?mol-1,依据盖斯定律②×6-①得到:
2CO2(g)+6H2(g)?CH3OCH3(g)+3H2O(l)△H=-259.8kJ?mol?1,写出以CO2、H2合成CH3OCH3的热化学方程式为:2CO2(g)+6H2(g)?CH3OCH3(g)+3H2O(l)△H=-259.8kJ?mol?1。
(2)15~20%的乙醇胺.(HOCH2CH2NH2)水溶液具有弱碱性,上述合成线路中用作C02吸收剂,乙醇胺水溶液呈弱碱性是取代基氨基结合氢离子,使溶液中的氢氧根离子浓度增大,结合二氧化碳生成碳酸盐,反应的化学方程式为:2HOCH2CH2NH2+H2O+CO2?(HOCH2CH2NH3)2CO3。
(3)生产0.3mol二甲醚,理论上应生成二甲醚物质的量0.3mol÷5%=6mol,反应的反应的CO2的物质的量为12mol,实际通入的CO2的物质的量为12mol÷60%=20mol。
(4)①反应本质是二甲醚的燃烧,原电池负极发生氧化反应,二甲醚在负极放电,正极反应还原反应,氧气在正极放电.由图可知,a极为负极,b为正极,二甲醚放电生成二氧化碳与氢离子,a电极的电极反应式为 CH3OCH3-12e-+3H2O═2CO2+12H+。
②若以1.12L?min-1(标准状况)的速率向该电池中通入二甲醚,用该电池电解500mL 2mol?L-1 CuS04溶液,通电0.50min后,通入二甲醚物质的量=1.12L/min×0.50min÷22.4L/mol
=0.025mol;依据电极反应电子守恒,CH3OCH3~12e-,n(e?)=0.025mol×12=0.3mol, 50mL2 mol·L-1 CuSO4溶液,Cu2+共0.05mol×2mol?L?1=0.1mol,Cu2+完全反应,所以m(Cu)=0.1mol×64g/mol=6.4g

练习册系列答案
 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案
相关题目
 H2(g)+
H2(g)+
 ,它所对应反应的化学方程式为 。
,它所对应反应的化学方程式为 。 CH3OH(g) △H1=-90.7kJ·mol-1
CH3OH(g) △H1=-90.7kJ·mol-1
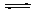 N2(g)+2CO2(g) △H<0。
N2(g)+2CO2(g) △H<0。