题目内容
(1)已知:① TiO2(s)+2Cl2(g)=TiCl4(l)+O2(g) ΔH=+140 kJ·mol-1
②2C(s)+O2(g)=2CO(g) ΔH=-221 kJ·mol-1
写出TiO2和焦炭、氯气反应生成液态TiCl4和CO气体的热化学方程式:________________。
(2)有一类甲醇质子交换膜燃料电池,需将甲醇蒸气转化为氢气,两种反应原理是:
A.CH3OH(g)+H2O(g)=CO2(g)+3H2(g) ΔH=+49.0 kJ·mol-1
B.CH3OH(g)+3/2O2(g)=CO2(g)+2H2O(g) ΔH=-676.7 kJ·mol-1
由上述方程式可知,CH3OH的标准燃烧热________(填“大于”“等于”“小于”或“不能确定”)-676.7 kJ·mol-1。已知水的气化热为44 kJ·mol-1,则氢气燃烧的热化学方程式为__________________________。
②2C(s)+O2(g)=2CO(g) ΔH=-221 kJ·mol-1
写出TiO2和焦炭、氯气反应生成液态TiCl4和CO气体的热化学方程式:________________。
(2)有一类甲醇质子交换膜燃料电池,需将甲醇蒸气转化为氢气,两种反应原理是:
A.CH3OH(g)+H2O(g)=CO2(g)+3H2(g) ΔH=+49.0 kJ·mol-1
B.CH3OH(g)+3/2O2(g)=CO2(g)+2H2O(g) ΔH=-676.7 kJ·mol-1
由上述方程式可知,CH3OH的标准燃烧热________(填“大于”“等于”“小于”或“不能确定”)-676.7 kJ·mol-1。已知水的气化热为44 kJ·mol-1,则氢气燃烧的热化学方程式为__________________________。
(1)TiO2(s)+2C(s)+2Cl2(g)=TiCl4(l)+2CO(g) ΔH=-81 kJ·mol-1
(2)不能确定 H2(g)+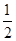 O2(g)=H2O(l) ΔH=-285.9 kJ·mol-1
O2(g)=H2O(l) ΔH=-285.9 kJ·mol-1
(2)不能确定 H2(g)+
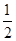 O2(g)=H2O(l) ΔH=-285.9 kJ·mol-1
O2(g)=H2O(l) ΔH=-285.9 kJ·mol-1 试题分析:(1)将①+②可得:TiO2(s)+2C(s)+2Cl2(g)=TiCl4(l)+2CO(g) ΔH=-81 kJ·mol-1
(2)由于A产物是氢气,不是化合物,B产物是气态的水,不是稳定的化合物的状态。所以不能确定CH3OH的标准燃烧热。将(A─B)÷3可得:H2(g)+1/2O2(g)=H2O(g) ΔH= -241.9KJ/mol.由于水的气化热为44 kJ·mol-1,所以氢气燃烧的热化学方程式为:H2(g)+
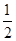 O2(g)=H2O(l) ΔH=-285.9 kJ·mol-1
O2(g)=H2O(l) ΔH=-285.9 kJ·mol-1 
练习册系列答案
相关题目



 ①
①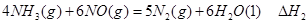 ②
② ③
③ 、
、 、
、 三者之间关系的表达式,
三者之间关系的表达式,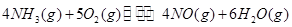
 =
=









 O2(g)= ZnO (s) △H=" -" Q1 kJ? mol-1 ①
O2(g)= ZnO (s) △H=" -" Q1 kJ? mol-1 ① O2(g)=ZnO(s) ΔH1=-351.1 kJ·mol-1
O2(g)=ZnO(s) ΔH1=-351.1 kJ·mol-1
