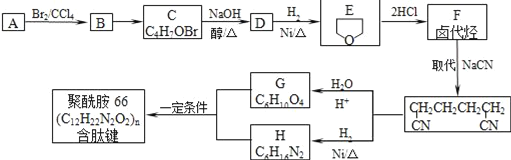
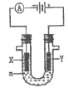
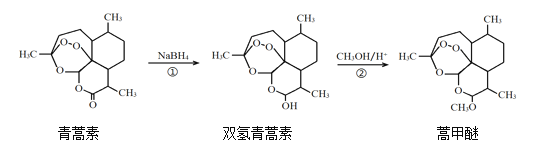
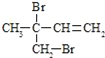��Ŀ����
����Ŀ�������裨Si3N4����һ����Ҫ���մɲ��ϣ�����ʯӢ�뽹̿��1400~1450��ĵ��������ºϳɣ�3SiO2(s)+6C(s)+2N2(g)![]() Si3N4(s)+6CO(g)-Q(Q>0)����һ�������£���10L�ܱ������м��뷴Ӧ�10min��ﵽƽ�⡣
Si3N4(s)+6CO(g)-Q(Q>0)����һ�������£���10L�ܱ������м��뷴Ӧ�10min��ﵽƽ�⡣
���������գ�
��1��������Ӧ���漰��Ԫ�أ�ԭ�Ӱ뾶�ɴ�С��˳����_____������һ��Ԫ�ص�ԭ�Ӻ���s��������p��������ȣ�д�����ĺ�������Ų�ʽ______��
��2��������Ӧ������еļ��Է�����______��д���Ǽ��Է��ӵĵ���ʽ______�������õ�����������кͷ����������Ȳ�����ԭ���ǣ�______��
��3�����д�ʩ������߶�������ת���ʵ���______��ѡ���ţ���
a.���ӽ�̿���� b.���߷�Ӧ�¶�
c.��������ѹǿ d.��Ӧ�����ж���뵪��
��4��������������˵����Ӧ�Ѵ�ƽ�����______��ѡ���ţ���
a.c(CO)=3c(N2) b.v(CO)=3v(N2)
c.������������ܶȲ��� d.�����ѹǿ���ֲ���
��5���÷�Ӧ��ƽ�ⳣ��Ϊ____��ƽ������ӵ���Ũ�ȣ�ƽ����______����������Ӧ�������淴Ӧ���������ƶ���Kֵ____���������������С���������������������ƽ��ʱ��������������11.2g�����õ�����ʾ��ƽ����Ӧ����Ϊ_____��
���𰸡�Si��C��N��O 1s22s22p4 CO ![]() ��������ԭ�Ӿ��壬�۵�� bd cd
��������ԭ�Ӿ��壬�۵�� bd cd ![]() ����Ӧ ���� 0.002molL-1min-1
����Ӧ ���� 0.002molL-1min-1
��������
��1��ͬ�����������ԭ�Ӱ뾶��С��ͬ�������϶���ԭ�Ӱ뾶����
����Ԫ���е�һ��Ԫ�ص�ԭ�Ӻ���s��������p��������ȣ�����������Ų���1s22s22p4��
��2��CO���ڼ��Է��ӣ�����Ϊ�Ǽ��Է��ӣ�����������Nԭ��֮���γ�3�Թ��õ��Ӷԣ���������ԭ�Ӿ��塢�۵�ߣ�
��3����߶�������ת���ʣ�Ӧ�ı�����ʹƽ�������ƶ������ƽ���ƶ���Ӱ�����ط������
��4�����淴Ӧ����ƽ��ʱ��ͬ�����ʵ�������������ұ��ֲ��䣬����ֵ�Ũ�ȡ��������ֲ��䣬�ɴ�����������һЩ�����䣬�ж�ƽ���������Ӧ�淴Ӧ���з����仯�����������ɱ仯�����ٱ仯˵������ƽ�⣻
��5�����ò������������ɲμӷ�Ӧ�������������ٸ���![]() ���м��㣻
���м��㣻
(1)ͬ�����������ԭ�Ӱ뾶��С��ͬ�������϶���ԭ�Ӱ뾶����ԭ�Ӱ뾶��Si>C>N>O��
����Ԫ���е�һ��Ԫ�ص�ԭ�Ӻ���s��������p��������ȣ�����������Ų�Ϊ1s22s22p4��
(2)CO���ڼ��Է���������Ϊ�ǽ����Է���������������Nԭ��֮���γ�3�Թ��õ��Ӷ�,����ʽΪ![]() ����������ԭ�Ӿ��塢�۵�ߣ��������췢���������Ȳ�����
����������ԭ�Ӿ��塢�۵�ߣ��������췢���������Ȳ�����
(3)a����̿Ϊ���壬���ӽ�̿������ƽ�ⲻ�ƶ���a����
b������ӦΪ���ȷ�Ӧ�����߷�Ӧ�¶�ƽ�������ƶ�����������ת��������b��ȷ��
c������ӦΪ�����������ķ�Ӧ����������ѹǿ��ƽ�������ƶ�����������ת���ʼ�С��c����
d����Ӧ�����ж���뷴Ӧ�ﵪ����ƽ�������ƶ�����������ת��������d��ȷ��
����bd��
(4)a��ƽ��ʱCO��������Ũ��֮�Ȳ�һ�����ڻ�ѧ������֮�ȣ�a����
b��![]() ��δָ���������ʣ�����Ϊ����Ӧ���ʣ���Ӧʼ�հ��ñ�����ϵ���У������ж�ƽ��״̬�����ֱ��ʾ��������ʱ�����жϷ�Ӧ����ƽ�⣬b����
��δָ���������ʣ�����Ϊ����Ӧ���ʣ���Ӧʼ�հ��ñ�����ϵ���У������ж�ƽ��״̬�����ֱ��ʾ��������ʱ�����жϷ�Ӧ����ƽ�⣬b����
c������![]() ���ڷ�Ӧ�ù��������������������ӣ�������䣬�����ܶȲ��������ǵ�ƽ��ʱ�������������䣬�ܶ�Ҳ���䣬���Կ��ж�ƽ��״̬��c��ȷ��
���ڷ�Ӧ�ù��������������������ӣ�������䣬�����ܶȲ��������ǵ�ƽ��ʱ�������������䣬�ܶ�Ҳ���䣬���Կ��ж�ƽ��״̬��c��ȷ��
d���淴Ӧ�����������ʵ��������º�����ѹǿ���������ѹǿ���ֲ��䣬˵����Ӧ����ƽ�⣬d��ȷ��
����cd��
(5)ƽ�ⳣ������ʽ��![]() ������Ӧ�ﵪ��Ũ��ʱ��ƽ���������ƶ������������¶�û�б仯������ƽ�ⳣ����С���䣻
������Ӧ�ﵪ��Ũ��ʱ��ƽ���������ƶ������������¶�û�б仯������ƽ�ⳣ����С���䣻
���ò���������μӷ�Ӧ��N2����Ϊx��
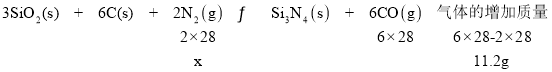
���![]() ����
����![]() �����㣺
�����㣺![]() ��
��

����Ŀ���������������������������ܹ��������·�Ӧ��MnO4-+H2C2O4+H+-Mn2++CO2��+H2O��δ��ƽ��
��ͬѧ�о�������ضԷ�Ӧ����Ӱ�죬�������ʵ�鷽����
��4mL0.001mol/LKMnO4��Һ��2mL0.01mol/LH2C2O4��Һ���о���ͬ�����Ի�ѧ��Ӧ���ʵ�Ӱ�죮�ı���������£�
��� | 10%�������/mL | �¶�/�� | �������� |
A | 2mL | 20 | |
B | 2mL | 20 | 10�α���MnSO4��Һ |
C | 2mL | 30 | |
D | 1mL | 20 | V1mL����ˮ |
E | 0.5mL | 20 | V2mL����ˮ |
��1���������ʵ�鷽����ƣ����У�V1= ______ ��V2= ______ ��
��2������о��¶ȶԻ�ѧ��Ӧ���ʵ�Ӱ�죬ʹ��ʵ�� ______ �� ______ ��
��3����ͬѧ����A��ʵ��ʱ�����ַ�Ӧ��ʼʱ���ʽ��������ӿ죮��������Ϊ��������� ������Һ�ķ�Ӧ���ȣ�������Һ�¶����ߣ���Ӧ���ʼӿ죻��Ӱ�컯ѧ��Ӧ���ʵ����ؿ�������뻹������ ______ ��
����ͬѧ������ͼ�ⶨ��Ӧ����
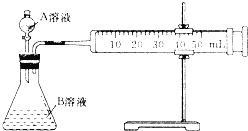
�ش���������
��4��ʵ��ʱҪ���װ�õ������ԣ����������ķ����� ______ ��
��5����ͬѧͨ��������ͬ�����CO2����ʾ��Ӧ�����ʣ���Ҫ ______ ������¼���ݣ�
����Ŀ����O2��HClת��ΪCl2����Ӧ����ʽΪ��4HCl(g) + O2(g)![]() 2H2O(g)+ 2Cl2(g)+Q��Q>0��һ�������²�÷�Ӧ������n(Cl2)��ʵ���������¡�����˵����ȷ���ǣ� ��
2H2O(g)+ 2Cl2(g)+Q��Q>0��һ�������²�÷�Ӧ������n(Cl2)��ʵ���������¡�����˵����ȷ���ǣ� ��
t/min | 0 | 2 | 4 | 6 |
n(Cl2)/10-3 mol | 0 | 1.8 | 3.7 | 5.4 |
A.0��2 min�ķ�Ӧ����С��4��6 min�ķ�Ӧ����
B.2��6 min��Cl2��ʾ�ķ�Ӧ����Ϊ0.9 mol/(L��min)
C.����ѹǿ�������HClת����
D.ƽ�ⳣ��K(200��)��K(400��)