题目内容
【题目】聚酰胺-66是含有肽键的高分子化合物,常用于生产帐篷、渔网等。可用以下方法合成:
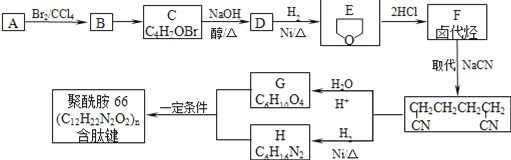
已知:A与E互为同分异构体,完成下列填空:
(1)A→B的反应类型______,A中含氧官能团的名称______
(2)B的结构简式______,D可能的结构简式______
(3)F与氢氧化钠的乙醇溶液共热得到烃I,I的名称______。比I多一个碳原子的同系物,与等物质的量溴反应生成二溴代物的结构简式正确的是______
a.![]()
b.![]()
c.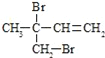
d.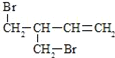
(4)G和H反应生成聚酰胺-66的化学方程式:______
(5)同时满足下列条件的G的同分异构体的结构简式为______
①含一种官能团 ②能发生银镜反应 ③含甲基且有三种化学环境不同的氢原子
【答案】加成反应 羟基 CH2BrCHBrCH2CH2OH ![]() 1,3﹣丁二烯 ac nHOOC(CH2)4COOH+nH2N(CH2)6NH2
1,3﹣丁二烯 ac nHOOC(CH2)4COOH+nH2N(CH2)6NH2![]() HO
HO![]() H+(2n-1)H2O HCOOCH(CH3)CH(CH3)OOCH
H+(2n-1)H2O HCOOCH(CH3)CH(CH3)OOCH
【解析】
由合成流程图可知,A能与溴发生加成反应,说明A中有不饱和键,B再生成C,C的分子式为C4H7OBr,C在NaOH醇溶液中发生消去反应生成D,D分子中有碳碳双键,D和H2加成得到E(![]() )。A与E互为同分异构体,则A的分子式为C4H8O,有一个碳碳双键,结合E的结构可推测,A是直链结构,结构简式为CH2=CHCH2CH2OH,所以B为CH2BrCHBrCH2CH2OH,C为
)。A与E互为同分异构体,则A的分子式为C4H8O,有一个碳碳双键,结合E的结构可推测,A是直链结构,结构简式为CH2=CHCH2CH2OH,所以B为CH2BrCHBrCH2CH2OH,C为![]() ,D为
,D为![]() ,E与2分子HCl反应得F,F与NaCN发生取代反应生成NCCH2CH2CH2CH2CN,F为ClCH2CH2CH2CH2Cl,NCCH2CH2CH2CH2CN水解得G为HOOCCH2CH2CH2CH2COOH,NCCH2CH2CH2CH2CN与氢气发生加成反应得H为H2NCH2CH2CH2CH2CH2CH2NH2,G和H发生缩聚反应得J聚酰胺-66,据此答题。
,E与2分子HCl反应得F,F与NaCN发生取代反应生成NCCH2CH2CH2CH2CN,F为ClCH2CH2CH2CH2Cl,NCCH2CH2CH2CH2CN水解得G为HOOCCH2CH2CH2CH2COOH,NCCH2CH2CH2CH2CN与氢气发生加成反应得H为H2NCH2CH2CH2CH2CH2CH2NH2,G和H发生缩聚反应得J聚酰胺-66,据此答题。
(1)根据上面的分析可知,A→B的反应类型为加成反应,A中含氧官能团的名称为羟基;
(2)根据上面的分析可知,B为CH2BrCHBrCH2CH2OH,D为![]() 或
或![]() ;
;
(3)F为ClCH2CH2CH2CH2Cl,F与氢氧化钠的乙醇溶液共热发生消去反应得到烃I为CH2=CHCH=CH2,I的名称为1,3-丁二烯,比I多一个碳原子的同系物为CH2=C(CH3)CH=CH2或CH2=CHCH=CHCH3或CH2=CHCH2CH=CH2,与等物质的量溴反应生成二溴代物为![]() 、
、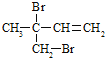 等,故选ac;
等,故选ac;
(4)G和H反应生成聚酰胺66的化学方程式为nHOOC(CH2)4COOH+nH2N(CH2)6NH2![]() HO
HO![]() H+(2n-1)H2O;
H+(2n-1)H2O;
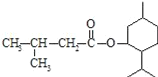
(5)G为HOOCCH2CH2CH2CH2COOH,根据条件①含一种官能团,②能发生银镜反应,说明含有醛基或甲酸某酯,③含甲基且有三种化学环境不同的氢原子,则符合条件的G的同分异构体的结构简式为 HCOOCH(CH3)CH(CH3)OOCH。

 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
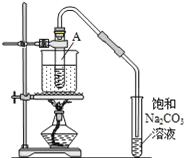
暑假作业安徽少年儿童出版社系列答案【题目】用下图所示装置进行下列实验:将①中溶液滴入②中,预测的现象与实际相符的是

选项 | ①中物质 | ②中物质 | 预测②中的现象 |
A. | 稀盐酸 | 碳酸钠与氢氧化钠的混合溶液 | 立即产生气泡 |
B. | 浓硝酸 | 用砂纸打磨过的铝条 | 产生红棕色气体 |
C. | 氯化铝溶液 | 浓氢氧化钠溶液 | 产生大量白色沉淀 |
D. | 草酸溶液 | 高锰酸钾酸性溶液 | 溶液逐渐褪色 |
【题目】制烧碱所用盐水需两次精制。
第一次精制主要是用沉淀法除去粗盐水中Ca2+、Mg2+、Fe3+、SO42-等离子,过程如下:
Ⅰ.向粗盐水中加入过量BaCl2溶液,过滤;
Ⅱ.向所得滤液中加入过量Na2CO3溶液,过滤;
Ⅲ.滤液用盐酸调节pH,获得一次精制盐水。
已知:过程Ⅰ、Ⅱ生成的部分沉淀及其溶解度(20℃/g)如表:
完成下列填空:
CaSO4 | Mg2(OH)2CO3 | CaCO3 | BaSO4 | BaCO3 |
2.6×10-2 | 2.5×10-4 | 7.8×10-4 | 2.4×10-4 | 1.7×10-3 |
(1)过程Ⅰ除去的离子是_______________。
(2)检测Fe3+是否除尽的方法是____________________。
(3)过程Ⅰ选用BaCl2而不选用CaCl2,请运用表中数据解释原因______________。
(4)除去Mg2+的离子方程式是________________。
(5)检测Ca2+、Mg2+、Ba2+是否除尽时,只需检测Ba2+即可,原因是_____________。
第二次精制要除去微量的I-、IO3-、NH4+、Ca2+、Mg2+,流程示意如图:
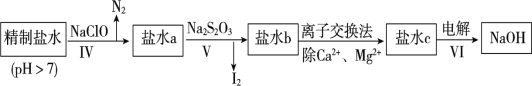
(6)过程Ⅳ除去的离子是__________________。
(7)过程VI中,在电解槽的阴极区生成NaOH,结合化学平衡原理解释___________。