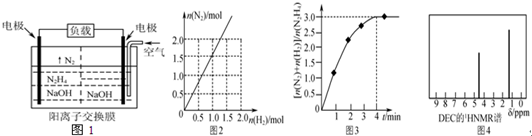
题目内容
4.某有机物T的分子式为C5H12O4,0.1mol T与足量钠反应生成4.48L(标准状况)氢气.已知一个碳原子上连接两个-OH的有机物不稳定.则T的稳定结构(不考虑立体异构)有( )| A. | 6种 | B. | 7种 | C. | 8种 | D. | 9种 |
分析 分子式为C5H12O4,0.1mol T与足量钠反应生成4.48L(标准状况)氢气即0.2mol氢气,即1mol T与足量钠反应生成4.48L(标准状况)氢气即2mol氢气,则说明C5H12O4中含4个-OH,已知一个碳原子上连接两个-OH的有机物不稳定,即4个-OH分别连在4个碳原子上,只有一个碳原子上不连-OH,据此分析.
解答 解:有机物的分子式为C5H12O4,0.1mol T与足量钠反应生成4.48L(标准状况)氢气即0.2mol氢气,即1mol T与足量钠反应生成4.48L(标准状况)氢气即2mol氢气,则说明C5H12O4中含4个-OH,已知一个碳原子上连接两个-OH的有机物不稳定,即4个-OH分别连在4个碳原子上,只有一个碳原子上不连-OH.
当这5个碳原子为正戊烷C-C-C-C-C的碳链结构时,这唯一一个不连-OH的碳原子的可能位置有3种,即4个-OH在此碳链上的连接方式有3种,即CH2(OH)CH(OH)CH(OH) CH(OH)CH3,CH2(OH)CH(OH)CH(OH)CH2CH2OH;CH2(OH)CH(OH)CH2CH(OH)CH2OH
当这5个碳原子为异戊烷的碳链结构时,这唯一一个不连-OH的碳原子的可能位置有4种,即4个-OH在此碳链上的连接方式有4种:(CH2OH)2C(OH)CH(OH)CH3,(CH2OH)2C(OH)CH2CH2OH;(CH2OH)2CHCH(OH)CH2OH,HOCH2CH(CH3)(OH)CH3CH(OH)CH2OH;
当这5个碳原子为新戊烷的碳链结构时,由于能连-OH的碳原子只有4个,故将4个-OH连在C原子上的连接方法只有1种,即C(CH2OH)4;
故T的稳定结构共有8种.
故选C.
点评 本题考查了同分异构体的书写,注意当有多个官能团时书写位置异构时的解题技巧,难度较大.

| A. | 乙醇能消毒杀菌 | |
| B. | 锌可用作锌锰干电池的负极材料 | |
| C. | 糖类、油脂、蛋白质均是有机高分子化合物 | |
| D. | 硅可用于制造太阳能光电池 |
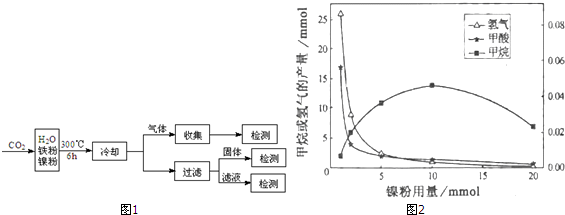
反应结束后,气体中检测到CH4和H2,滤液中检测到HCOOH,固体中检测到镍粉和Fe3O4.CH4、HCOOH、H2的产量和镍粉用量的关系如图2所示(仅改变镍粉用量,其他条件不变):研究人员根据实验结果得出结论:HCOOH是CO2转化为CH4的中间体,即:CO2$\stackrel{Ⅰ}{→}$HCOOH$\stackrel{Ⅱ}{→}$CH4.由图可知,镍粉是反应Ⅰ、Ⅱ的催化剂,当镍粉用量从1mmol增加到10mmol,反应速率的变化情况是( )
| A. | 反应Ⅰ的速率增加,反应Ⅱ的速率不变 | |
| B. | 反应Ⅰ的速率不变,反应Ⅱ的速率增加 | |
| C. | 反应Ⅰ、Ⅱ的速率均增加,且反应Ⅰ的速率增加得快 | |
| D. | 反应Ⅰ、Ⅱ的速率均增加,且反应Ⅱ的速率增加得快 |
| A. | 金属腐蚀的本质是金属原子失去电子而被氧化 | |
| B. | 钢铁吸氧腐蚀的正极反应是:O2+4e-+2H2O=4OH- | |
| C. | 氢氧燃料电池中,氢气在负极发生氧化反应 | |
| D. | 将地下钢管与直流电源的正极相连,用来保护钢管 |
| A. | 常温下,将pH=3的醋酸溶液稀释到原体积的10倍后,溶液的pH=4 | |
| B. | 用0.2000 mol/L NaOH标准溶液滴定HCl与CH3COOH的混合液(混合液中两种酸的浓度均约为0.1 mol/L),至中性时,溶液中的酸未被完全中和 | |
| C. | 相同条件下,2mol氢原子所具有的能量小于1mol氢分子所具有的能量 | |
| D. | 相同温度下,将足量氯化银固体分别放入相同体积的①蒸馏水、②0.1 mol/L盐酸、③0.1 mol/L氯化镁溶液、④0.1 mol/L硝酸银溶液中,Ag+浓度:①>④=②>③ |
| A. | NaCl常用于保存食物 | |
| B. | 烹鱼时加入少量酒、食醋,美味又营养 | |
| C. | 糖类、油脂、蛋白质均为高分子化合物 | |
| D. | 燃煤中加入CaCO3,可减少SO2气体对大气的污染 |
| A. | MgO | B. | NaCl | C. | SiO2 | D. | K2S |
 .
.