题目内容
8.工业上利用硫酸渣(含Fe2+、Fe3+的硫酸盐及少量CaO和MgO)制备高档颜料铁红(Fe2O3)和回收(NH4)2SO4,具体生产流程如下: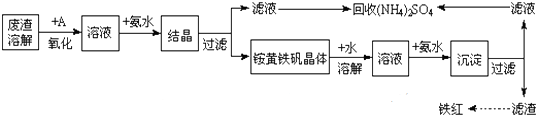
(注:铵黄铁矾化学式为(NH4)2Fe6(SO4)4(OH)12)
(1)在废渣溶解操作时,应选用D溶解(填字母).
A、氨水 B、氢氧化钠 C、盐酸 D、硫酸
(2)物质A是一种氧化剂,工业上最好选用空气(供选择使用的有:空气、Cl2、MnO2),其理由是原料来源容易,成本低,不产生污染,不引入杂质.
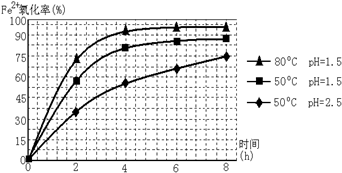
(3)根据图有关数据,你认为工业上氧化操作时应控制的条件是:溶液温度控制在80℃,pH控制在1.5.
(4)“结晶”反应的化学方程式为3Fe2(SO4)3+2NH3.H2O+10H2O=(NH4)2Fe6(SO4)4(OH)12↓+5H2SO4.
(5)简述检验“滤液”中含有NH4+的实验方法:取少量滤液于试管中,向试管中加入足量的浓氢氧化钠溶液,加热.用湿润的红色石蕊试纸放在试管口处,红色石蕊试纸变蓝色,说明滤液中含有NH4+.
分析 将废渣溶解,溶解时加入的物质能溶解废渣但不能引进杂质;然后向溶液中加入A,A具有氧化性,能氧化亚铁离子但不能引进新的杂质且原料易得、成本低;然后向溶液中加入氨水,溶液中硫酸铁和氨水反应生成铵黄铁矾,采用过滤方法分离得到铵黄铁矾和滤液;将滤液蒸发浓缩回收硫酸铵;
将铵黄铁矾溶于水得到溶液,然后向溶液中加入氨水,得到氢氧化亚铁沉淀,然后过滤得到滤渣,将滤渣加热得到铁红,
(1)溶解废渣的溶剂能溶解废渣且不能引进新的杂质;
(2)A是氧化剂,具有氧化性,能氧化亚铁离子,但不能引进新的杂质且原料易得、成本低;
(3)相同pH时,温度越高,亚铁离子的氧化率越大;相同温度时,pH越小,亚铁离子的氧化率越大;
(4)硫酸铁和一水合氨反应生成铵黄铁矾和硫酸;
(5)铵根离子和氢氧根离子生成一水合氨,加热生成氨气,氨气能够使湿润的红色石蕊试纸变蓝.
解答 解:将废渣溶解,溶解时加入的物质能溶解废渣但不能引进杂质;然后向溶液中加入A,A具有氧化性,能氧化亚铁离子但不能引进新的杂质且原料易得、成本低;然后向溶液中加入氨水,溶液中硫酸铁和氨水反应生成铵黄铁矾,采用过滤方法分离得到铵黄铁矾和滤液;将滤液蒸发浓缩回收硫酸铵;
将铵黄铁矾溶于水得到溶液,然后向溶液中加入氨水,得到氢氧化亚铁沉淀,然后过滤得到滤渣,将滤渣加热得到铁红,
(1)溶解废渣的溶剂能溶解废渣且不能引进新的杂质,氨水和NaOH不溶解CaO和MgO,稀盐酸能溶解废渣但引进杂质,稀硫酸能溶解废渣且不引进新的杂质,故选D;
(2)A是氧化剂,具有氧化性,能氧化亚铁离子,但不能引进新的杂质且原料易得、成本低,氯气和二氧化锰都具有氧化性,但引进新的杂质且成本高,所以选取空气,
故答案为:空气;原料来源容易,成本低,不产生污染,不引入杂质;
(3)相同pH时,温度越高,亚铁离子的氧化率越大;相同温度时,pH越小,亚铁离子的氧化率越大,根据图知,溶液温度控制在80℃,pH控制在1.5,氧化时间为4小时左右,所以控制的条件是:溶液温度控制在80℃,pH控制在1.5,故答案为:溶液温度控制在80℃,pH控制在1.5;
(4)硫酸铁和一水合氨反应生成铵黄铁矾和硫酸,反应方程式为3Fe2(SO4)3+2NH3.H2O+10H2O=(NH4)2Fe6(SO4)4(OH)12↓+5H2SO4,
故答案为:3Fe2(SO4)3+2NH3.H2O+10H2O=(NH4)2Fe6(SO4)4(OH)12↓+5H2SO4;
(5)铵根离子和氢氧根离子生成一水合氨,加热生成氨气,氨气能够使湿润的红色石蕊试纸变蓝,铵根离子的检验方法是:取少量滤液于试管中,向试管中加入足量的浓氢氧化钠溶液,加热.用湿润的红色石蕊试纸放在试管口处,红色石蕊试纸变蓝色,说明滤液中含有NH4+,
故答案为:取少量滤液于试管中,向试管中加入足量的浓氢氧化钠溶液,加热.用湿润的红色石蕊试纸放在试管口处,红色石蕊试纸变蓝色,说明滤液中含有NH4+.
点评 本题考查物质分离和提纯,为高频考点,涉及离子检验、除杂、条件控制、氧化还原反应等知识点,综合性较强,明确流程图中发生的反应及基本操作方法是解本题关键,注意选取试剂时不能引进新的杂质.

| A. | 所有放热反应均是自发反应,也是熵增大的反应 | |
| B. | 向AgCl固液混合物中滴入KI饱和溶液,有AgI沉淀生成,说明AgCl的溶解度小于有AgI的溶解度 | |
| C. | 锌与稀硫酸反应制取氢气,加入少量的硫酸铜粉末会使产生氢气的速度减慢 | |
| D. | 用电解法精炼粗铜时,粗铜板作阳极,纯铜板作阴极 |
| A. | 1:1 | B. | 1:2 | C. | 2:1 | D. | 3:1 |
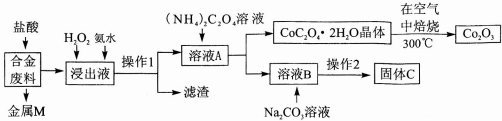
(1)金属M为Cu,操作1为过滤.
(2)加入H2O2的作用是(用离子方程式表示)2Fe2++H2O2+2H+=2Fe3++2H2O,加入氨水的作用是调节溶液的pH使Fe3+转化为Fe(OH)3沉淀.
(3)充分焙烧的化学方程式为4CoC2O4?2H2O+3O2焙烧_2Co2O3+8 H2O+8CO2.
(4)已知Li2CO3微溶于水,其饱和溶液的浓度与温度关系见下表.操作2中,蒸发浓缩后必须趁热过滤,其原因是减少Li2CO3的溶解损失,90℃时Ksp(Li2CO3)的值为4.0×10-3.
| 温度/℃ | 10 | 30 | 60 | 90 |
| 浓度/mol•L-1 | 0.21 | 0.17 | 0.14 | 0.10 |
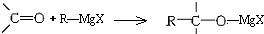 ,所得产物经水解可以得到醇,这是某些复杂醇的合成方法之一.现欲合成(CH3)3C-OH,下列所选用的卤代烃和羰基化合物的组合正确的是( )
,所得产物经水解可以得到醇,这是某些复杂醇的合成方法之一.现欲合成(CH3)3C-OH,下列所选用的卤代烃和羰基化合物的组合正确的是( )| A. | 乙醛和氯乙烷 | B. | 甲醛和1-溴丙烷 | C. | 甲醛和2-溴丙烷 | D. | 丙酮和一氯甲烷 |
| A. | 反应中Cu2S只做还原剂 | |
| B. | 参加反应的n(Cu2S):n(HNO3)=1:5 | |
| C. | 产物n[Cu(NO3)2]:n[CuSO4]=1:1 | |
| D. | 1 molCu2S参加反应时有10 mol电子转移 |
| A. | 1mol•L-1•min-1 | B. | 1.2mol•L-1•min-1 | ||
| C. | 6mol•L-1•min-1 | D. | 0.41mol•L-1•min-1 |