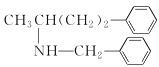题目内容
【题目】有容积不同的X、Y两密闭容器,X中充满CO气体,Y中充满CH4、O2、N2的混合气体,同温同压下测得两容器中气体密度相同。下列叙述中不正确的是
A.Y容器中CH4、O2、N2的质量之比可以为1∶6∶3
B.Y容器中CH4、O2、N2的物质的量之比一定为1∶3∶6
C.两容器中所含气体分子数一定不同
D.两容器中所含气体的质量一定不同
【答案】B
【解析】
A、两容器气体密度相同,将pV=nRT化为![]() ,可得同温同压下,ρ与M成正比,所以两容器中气体平均摩尔质量相同,即CH4、O2、N2的平均摩尔质量为28g/mol。由于N2的分子量为28g/mol,则CH4、O2的平均摩尔质量为28g/mol,设CH4的质量为xg,O2的质量为yg,则
,可得同温同压下,ρ与M成正比,所以两容器中气体平均摩尔质量相同,即CH4、O2、N2的平均摩尔质量为28g/mol。由于N2的分子量为28g/mol,则CH4、O2的平均摩尔质量为28g/mol,设CH4的质量为xg,O2的质量为yg,则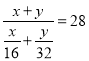 ,所以
,所以![]() ,N2的质量不固定,所以CH4、O2、N2的质量之比可以为1∶6:3,故A正确;B、根据选项A的分析可知,只要保证CH4、O2的质量之比为1∶6,即物质的量之比为1∶3,则可保证三者平均摩尔质量为28g/mol,故三者比值不是一个定值,故B错误;C、同温同压下,PV=nRT,两个容器的体积不同,则物质的量不同,所以分子数不同,故C正确;D、已知两个容器的体积不同,而气体的密度相同,由m=ρV可知,质量不同,故D正确。故选B。
,N2的质量不固定,所以CH4、O2、N2的质量之比可以为1∶6:3,故A正确;B、根据选项A的分析可知,只要保证CH4、O2的质量之比为1∶6,即物质的量之比为1∶3,则可保证三者平均摩尔质量为28g/mol,故三者比值不是一个定值,故B错误;C、同温同压下,PV=nRT,两个容器的体积不同,则物质的量不同,所以分子数不同,故C正确;D、已知两个容器的体积不同,而气体的密度相同,由m=ρV可知,质量不同,故D正确。故选B。

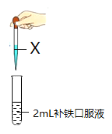
【题目】某研究小组同学对市售某种补铁口服液的成分进行探究。根据名称认为该糖浆中含有Fe2+,设计方案进行验证。

I.设计方案如下:
| 方案 | 试剂X | 预期现象 |
方案i | 1mL 1 mol/L NaOH溶液 | a | |
方案ii | 1mL 1 mol/L 酸性KMnO4溶液 | b | |
方案iii | 依次加入5滴KSCN溶液、1mL氯水 | c |
(1)方案i的预期现象是产生白色沉淀,逐渐变为灰绿色,最终变为红褐色。产生白色沉淀的离子方程式是_________,最终变为红褐色的化学方程式是________。
(2)方案ii的预期现象是_________。
(3)方案iii的预期现象是________,反应中氯水参与反应的的离子方程式是____。
II.进行实验操作,得到的实际现象如下:
方案 | 实际现象 | 是否与预期现象相同 |
方案i | 产生灰绿色浑浊,长时间不变红褐色 | 不同 |
方案ii | 相同 | |
方案iii | 自始至终无明显现象 | 不同 |
(4)为探究实验中出现异常现象的原因,该小组同学查看说明书,得知有关补铁口服液成分的如下:
本品每毫升含主要成分葡萄糖酸亚铁30毫克,
辅料为:蔗糖、香精、枸檬酸、羟苯乙酯。
结合资料对异常现象产生的原因进行猜想:______________;为验证其猜想,在方案iii的基础上继续加入过量的氯水,得到了预期的现象。
(5) 实验反思:方案ii中预期现象与实验现象相同,并不能证明补铁口服液中一定含有Fe2+,理由是______。
(6)小组同学进一步提出研究问题:仍选用之前用过的试剂,设计实验验证某久置的补铁口服液(计为Y
实验序号 | 操作 | 现象 |
ⅳ | 取2 mL溶液Y,加入1滴KSCN,再加入1 mL水 | 溶液显红色 |
V |
实验V的操作及现象是_____________。