题目内容
【题目】下列实验不合理的是
A. 证明非金属性强弱 S>C>Si 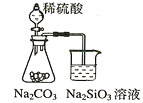
B. 四氯化碳萃取碘水中的碘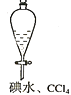
C. 制备并收集少量NO气体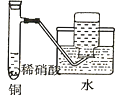
D. 制备少量氧气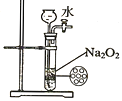
【答案】D
【解析】
A.发生的反应为Na2CO3+H2SO4=Na2SO4+H2O+CO2![]() ,CO2+Na2SiO3+H2O=H2SiO3+Na2CO3,证明酸性顺序H2SO4> H2CO3> H2SiO3,即非金属性强弱S>C>Si ,故A项正确;B.四氯化碳萃取碘水中的碘在分液漏斗中进行,故B项正确;C.3Cu+8HNO3(稀)=3Cu(NO3)2 +2NO
,CO2+Na2SiO3+H2O=H2SiO3+Na2CO3,证明酸性顺序H2SO4> H2CO3> H2SiO3,即非金属性强弱S>C>Si ,故A项正确;B.四氯化碳萃取碘水中的碘在分液漏斗中进行,故B项正确;C.3Cu+8HNO3(稀)=3Cu(NO3)2 +2NO![]() +4H2O,NO不溶于水,该装置可以制备并收集少量NO气体,故C正确。D.Na2O2遇水即溶解反应,不能留在筛孔上,无法做到随关随停,故D错误;答案D。
+4H2O,NO不溶于水,该装置可以制备并收集少量NO气体,故C正确。D.Na2O2遇水即溶解反应,不能留在筛孔上,无法做到随关随停,故D错误;答案D。

【题目】硫氧化物易引起环境行染,需要悉心研究。
(1)二氧化硫可用于催化氧化制硫酸。硫酸工业中,作为催化剂的V2O5对反应I的催化循环过程经历了Ⅱ、Ⅲ两个反应阶段,如图所示:

下列分子中1mol化学键断裂时需要吸收的能量数据如下:
化学键 | S=O(SO2) | S=O(SO3) | O=O(O2) |
能量/kJ | 535 | a | 496 |
反应Ⅰ的△H=-98 kJ ·mol-1,则 a=____________。反应Ⅲ的化学方程式为______________。将2molSO2和1molO2充入密闭容器中,在一定条件下发生反应:2SO2(g)+O2(g)![]() 2SO3(g)。平衡时SO3的体积分数(% )随温度和压强的变化如表所示:下列判断正确的是(_____________)
2SO3(g)。平衡时SO3的体积分数(% )随温度和压强的变化如表所示:下列判断正确的是(_____________)
压强/MPa 体积分数/% 温度/℃ | 1.0 | 2.0 | 3.0 |
350 | 5.0 | a | b |
415 | c | 40.0 | d |
550 | e | f | 36.0 |
A.b >e
B.415℃、2.0MPa时O2的转化率为60%
C.在一定温度和压强下,加入V2O5作催化剂能加快反应速率,提高SO3的体积分数
D.平衡常数K(550℃)>K(350℃)
(2)较纯的SO2,可用于原电池法生产硫酸。图中离子交换膜是________离子交换膜(填“阴”、“阳”)。

(3)研究发现,含碱式硫酸铝的溶液与SO2结合的方式有2种:其一是与溶液中的水结合。其二是与碱式硫酸铝中的活性Al2O3结合,通过酸度计测定吸收液的pH变化,结果如右图所示:

请解释曲线如图变化的原因_______________________________。
(4)取五等份SO3,分别加入温度不同、容积相同的恒容密闭容器中,发生反应:3SO3(g)![]() (SO3)3(g) △H<0,反应相同时间后,分别测定体系中SO3的百分含量,并作出其随反应温度(T)变化的关系图。下列示意图中,可能与实验结果相符的是(_____)
(SO3)3(g) △H<0,反应相同时间后,分别测定体系中SO3的百分含量,并作出其随反应温度(T)变化的关系图。下列示意图中,可能与实验结果相符的是(_____)

(5)用Na2SO3溶液作为吸收液吸收SO2时,产物为NaHSO3,已知亚硫酸的两级电离平衡常数分别为Ka1、Ka2。则常温下NaHSO3溶液显酸性的充要条件为_____________。(用含为Ka1、Ka2的代数式表示)








